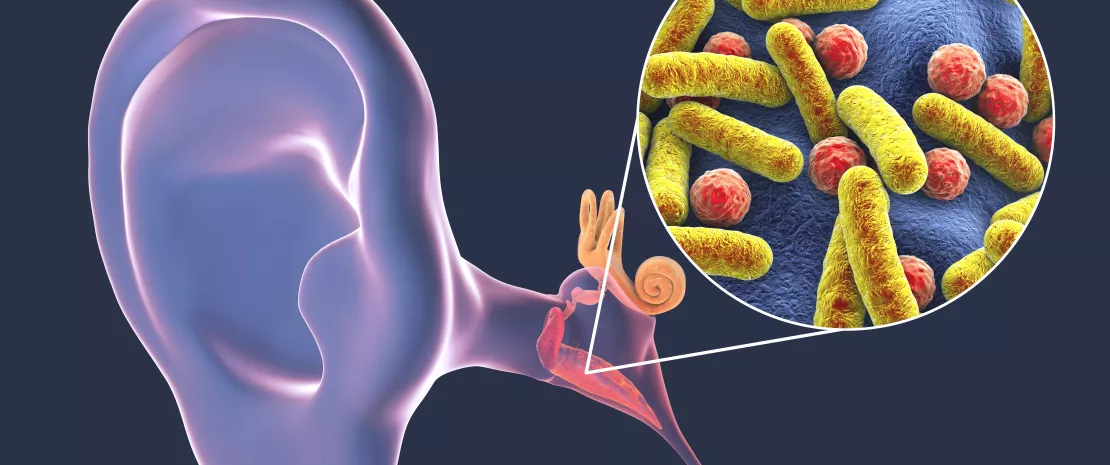
Długo uważana za sterylną jama macicy tak naprawdę jest domem mikrobioty złożonej z bakterii. Jest ich od 100 do 10 000 razy mniej niż w pochwie, ale też mają wpływ na stan zdrowia reprodukcyjnego. Tak sugeruje wieloośrodkowe (13 ośrodków zlokalizowanych w Europie, Ameryce i Azji) perspektywiczne badanie obserwacyjne, którego przedmiotem była analiza składu mikrobioty endometrialnej 342 bezpłodnych kobiet objętych programami zapłodnienia in vitro (IVF).
Dwie próbki mikrobioty endometrialnej
Przed przeniesieniem zarodka pobrano dwie próbki w celu oceny składu mikrobioty endometrium: próbkę płynu endometrialnego z jamy macicy i próbkę błony śluzowej pobranej metodą biopsji. Następnie naukowcy zbadali relacje między składem tej mikrobioty, analizowanym metodą sekwencjonowania RNA 16 S, a wynikiem IVF, czyli ciążą donoszoną (41% pacjentek), ciążą biochemiczną (8%), poronieniem (8%) lub brakiem ciąży (42%).
Dysbioza endometrialna ma związek z niepowodzeniem IVF
Badacze zaobserwowali zwiększoną liczebność bakterii z rodzaju Lactobacillus (w próbkach płynu i błony śluzowej) u pacjentek w ciąży donoszonej. Natomiast spadek liczebności bakterii Lactobacillus występujący jednocześnie ze specyficznym układem, w którym występują niektóre rodzaje potencjalnie chorobotwórczych bakterii, w tym Atopobium, Bifidobacterium, Chryseobacterium, Gardnerella, Haemophilus, Klebsiella, Neisseria, Staphylococcus i Streptococcus, ma związek z niepowodzeniem IVF lub brakiem rozwiązania ciąży w postaci narodzin zdolnego do życia dziecka. Należy zauważyć, że Gardnerella i Klebsiella były nadreprezentowane zarówno w płynie, jak i w endometrialnej błonie śluzowej pacjentek, u których procedura nie powiodła się.
Pałeczki kwasu mlekowego – mur obronny przeciw patogenom?
Dane te wskazują na rolę mikrobioty endometrialnej w powodzeniu lub niepowodzeniu implantacji zarodka i/lub przebiegu ciąży u pacjentek korzystających z IVF. Badacze stawiają hipotezę, że na wynik IVF bardziej może wpływać nieobecność w endometrium bakterii chorobotwórczych niż obecność bakterii korzystnych (takich jak pałeczki kwasu mlekowego). Bakterie Lactobacillus utrudniałyby w tym przypadku kolonizację jamy macicy przez bakterie chorobotwórcze. Wyjaśnienie mechanizmów działania bakterii chorobotwórczych wymaga dodatkowych badań.
Polecane przez naszą społeczność