Co trzeba z tego wynieść? Odporność jelit
Wywiad z ekspertem: Prof. Brigitte Dréno
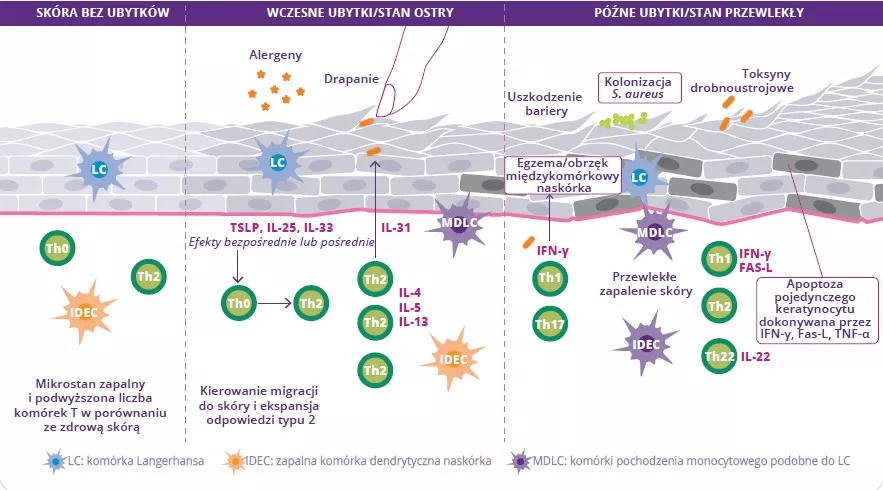
Atopowe zapalenie skóry (AZS) to przewlekła zapalna choroba skóry charakteryzująca się okresowymi nawrotami. Podobnie jak astma, katar sienny lub alergiczne zapalenie spojówek jest uznawane za chorobę alergiczną. Powoduje sączące się czerwone ubytki o nieregularnym kształcie występujące w określonych miejscach na skórze, na przykład w zgięciach łokci albo za kolanami, ale także na twarzy i reszcie ciała. AZS zwykle pojawia się w wczesnym dzieciństwie. Może przetrwać aż do dorosłości. Przyczyny są wieloczynnikowe i złożone. Obejmują predyspozycje genetyczne (mutacja filagryny – białka skóry), naruszenie bariery skórnej, dysbiozę mikrobioty skóry i jelit oraz rozregulowanie układu odpornościowego.
W krajach „rozwiniętych” AZS dotyka 15–20% dzieci i 10% dorosłych. W ostatnich dziesięcioleciach liczba przypadków znacznie wzrosła z powodu zanieczyszczenia i kontaktu z alergenami.1
Czy należy celować w mikrobiotę jelit żeby zoptymalizować skuteczność szczepionek?
Dr Genelle Healey
Hipoteza higieniczna a pandemia COVID-19
Dr Genelle Healey
Oś jelito-płuca w wirusowych infekcjach dróg oddechowych
Dr Genelle Healey
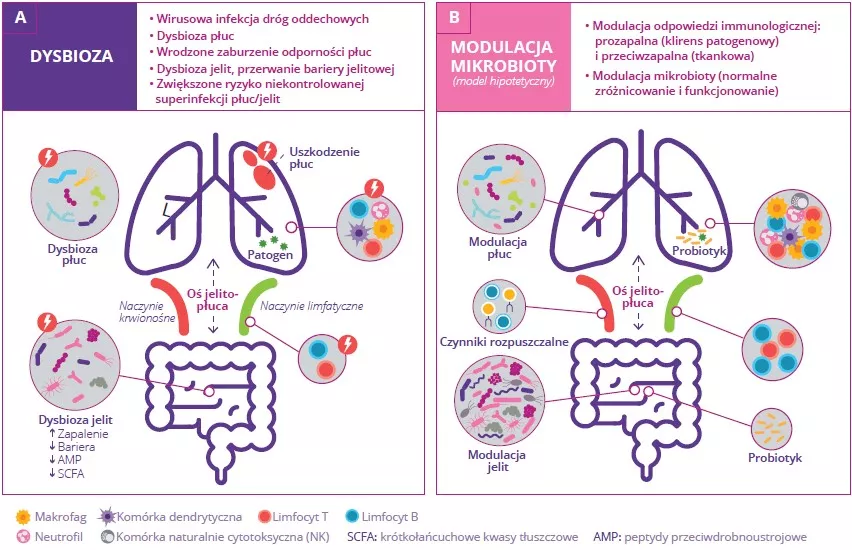
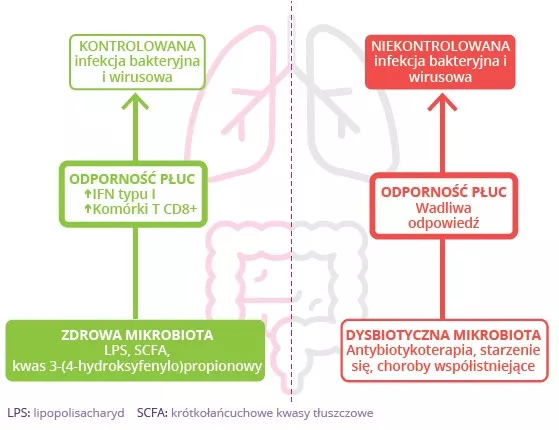
Mikrobiota jelit ma udział w obronie płuc przed wirusowymi infekcjami dróg oddechowych
Mikrobiota gra kluczową rolę w rozwoju, kształtowaniu i funkcjonowaniu układu odpornościowego zarówno na poziomie miejscowym, jak i ogólnoustrojowym. Mikrobiota dróg oddechowych reguluje funkcjonowanie układu odpornościowego na poziomie miejscowym, ale mikrobiota jelit również może wpływać na odporność układu oddechowego za pośrednictwem osi jelitopłuca.1 W przebiegu wielu chorób układu oddechowego zaobserwowano zaburzenie mikrobioty płucnej i jelitowej, ale trzeba jeszcze ustalić, czy dysbioza w tych narządach jest przyczyną, czy konsekwencją choroby.2 Zaburzenie składu mikrobioty jelit przez dietę, stosowanie antybiotyków,
starzenie się lub chorobę ma związek z zaburzeniem odpowiedzi immunologicznych i homeostazy dróg oddechowych,3 co wskazuje, że mikrobiota jelit może wpływać na rozwój chorób w całym organizmie, w tym również infekcji dróg oddechowych ( (Fig 6).4

Łagodzenie stanów zapalnych zoladka i jelit dieta
Dr Genelle Healey

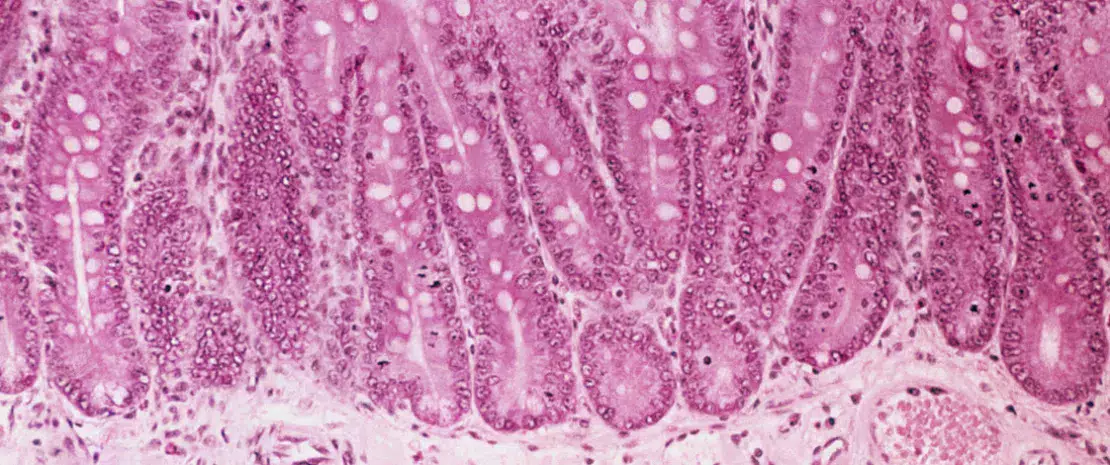
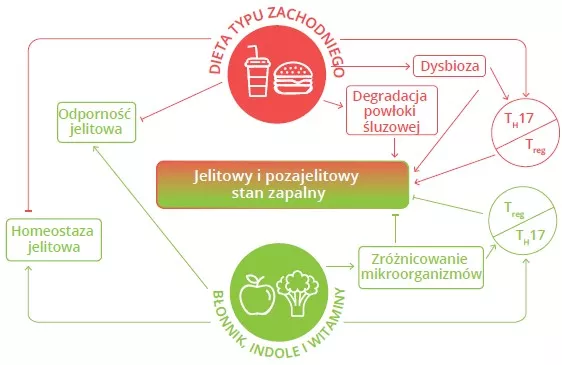
Wpływ diety zachodniej na powłokę śluzową
Dr Larissa Celiberto

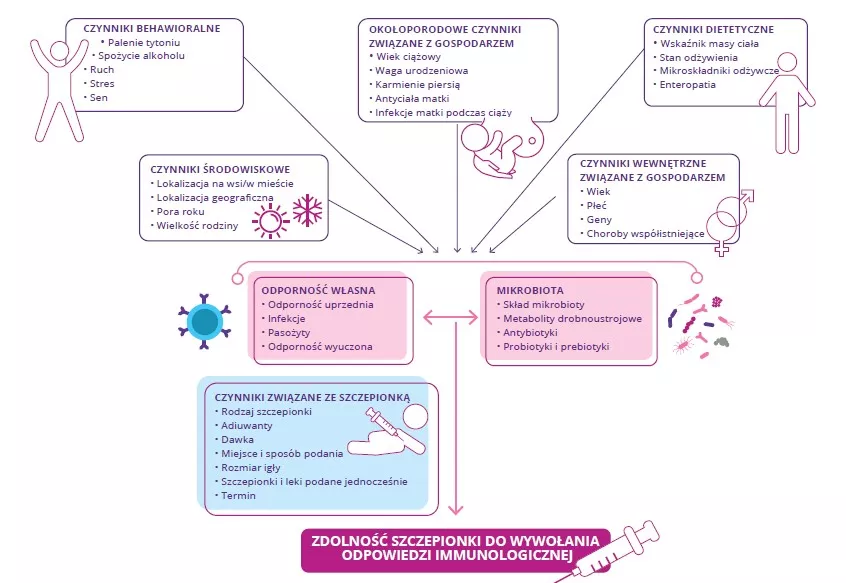
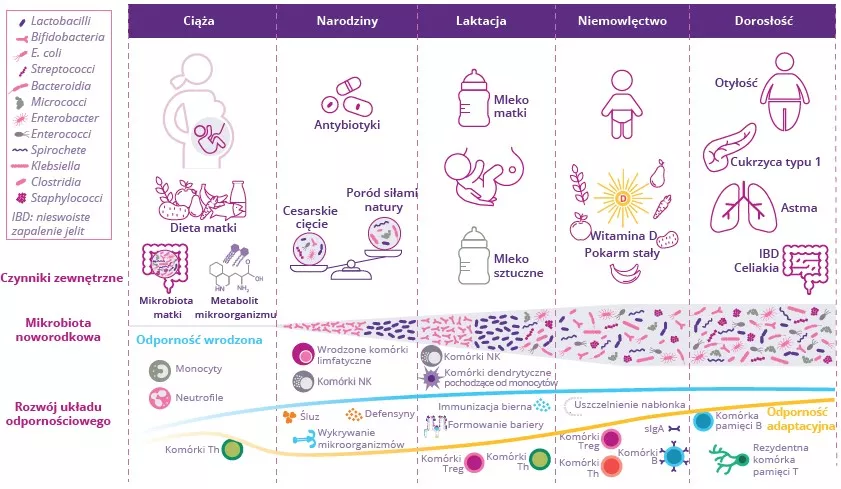
Czynniki wpływające na rozwój mikrobioty i dojrzewanie układu odpornosciowego na wczesnym etapie życia
Narodziny to największa zmiana w środowisku w ciągu życia ludzkiego, ponieważ noworodek po raz pierwszy styka się z niezliczonymi rodzajami mikroorganizmów kolonizujących wszystkie powierzchnie jego ciała, prowadząc do stworzenia mikrobioty komensalnej równolegle z powstaniem układu odpornościowego. Na skład mikrobioty jelit oraz dojrzewanie układu odpornościowego noworodka wpływa wiele czynników (rys. 3). Zakłócenia komunikacji między mikrobiotą a odpornością na poszczególnych etapach rozwoju mogą mieć długofalowy wpływ na podatność na choroby.13