Jelito noworodka: fundament odpornosci
Dr Travis J. De Wolfe
Rozwój wrodzonych barier immunologicznych
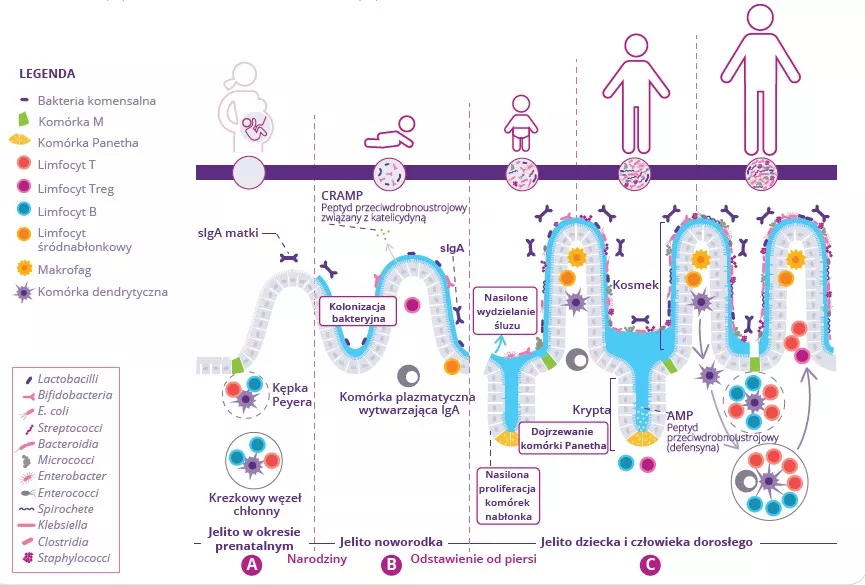
Rozwój jelitowego układu odpornościowego zaczyna się przed urodzeniem i trwa do czasu zaprzestania karmienia piersią. W okresie płodowym powstają niedojrzałe struktury układu limfatycznego, między innymi kępki Peyera i krezkowe węzły chłonne (rys. 1A). Struktury te dopiero na późniejszym etapie rozwoju stają się w pełni zdolne do funkcjonowania, dlatego w celu kompensacji braku ich działania nabłonek jelita wytwarza peptydy przeciwdrobnoustrojowe (AMP) działające jak bariera obronna reagująca na pierwsze kolonizujące bakterie (rys. 1B).1 Śluz jest kolejną ważną strukturą barierową wytwarzaną przez komórki kubkowe i wydzielaną na powierzchni apikalnej przewodu pokarmowego. Łącznie te wrodzone bariery immunologiczne grają kluczową rolę w ograniczeniu kontaktu mikrobioty jelit z komórkami nabłonka gospodarza, zwłaszcza gdy mikrobiota osadza się w jelicie niemowlęcia.
80% Co najmnie 80% komórek wytwarzających Ig znajduje się w jelicie.
Adaptacyjny układ odpornościowy noworodka również ma w okresie rozwoju krytyczne znaczenie
Wytwarzana jest immunoglobulina A (IgA) o różnym powinowactwie do składników mikrobioty oraz specyficznych antygenów żywnościowych spożywanych przez noworodka. Wydzielana IgA działa tak, aby wiązać te cele w świetle jelita i ograniczyć ich zdolność do przylegania do nabłonka jelita i/lub wnikania do niego (rys. 1B).2 W związku z tym w okresie odstawienia od piersi mikrobiota jelit noworodka staje się coraz bardziej zróżnicowana i skoncentrowana w odpowiedzi na zmianę diety i rozwój architektury kosmków i krypt. Wymaga to dalszej ochrony bariery nabłonkowej poprzez dojrzewanie miejscowych struktur układu limfatycznego. Pobudzone komórki Panetha zaczynają wytwarzać białka obronne gospodarza (defensyny) u podstawy małych krypt jelitowych, umożliwiając innym komórkom nabłonka zaprzestanie wytwarzania AMP. Na końcu proliferacja komórek nabłonka wzrasta razem z nasilonym wydzielaniem śluzu (rys. 1C).
RYSUNEK 1: Rozwój mikrobioty jelit i jelitowego układu immunologicznego przed urodzeniem (A) oraz przed (B) i po odstawieniu od piersi (C).
Adaptacja na podstawie Brandtzaeg P, 20173 and Ximenez C et al, 20176
Znaczenie homeostazy jelit
Co najmniej 80% komórek organizmu wytwarzających Ig znajduje się w jelicie.3 Jest to największy efektor odporności humoralnej. Wyspecjalizowane komórki nabłonka pobierające antygeny (komórki M) pełnią funkcje selekcyjne: ułatwiają transport antygenów pochodzących z bakterii komensalnych, diety lub patogenów ze światła jelita do położonych głębiej komórek układu limfatycznego. Następnie antygeny te są trawione przez komórki dendrytyczne (DC) i prezentowane adaptacyjnemu układowi immunologicznemu.
Poszczególne elementy odporności jelitowej razem wspierają homeostazę za pośrednictwem dwóch strategii przeciwzapalnych (rys. 1C):
1) wykluczenia immunologicznego obcych antygenów ogranicza/zapobiega kolonizacji błony śluzowej jelit przez mikrobiotę jelit; Tę funkcję pełni sIgA;3
2) tolerancja pokarmowa ogranicza miejscowe i obwodowe reakcje immunologiczne na nieszkodliwe antygeny wchodzące w kontakt z barierą nabłonkową.4 Zależy to od komórek Treg pełniących funkcje regulacyjne (rys. 2).3
Jeżeli strategie te funkcjonują prawidłowo, regulacja układu immunologicznego wraz z działaniem mikrobioty komensalnej wpływającej na rozwój i trening tego systemu prowadzi do stworzenia trwałej, homeostatycznej relacji gospodarza z organizmamikomensalnymi, która ma długofalowe implikacje dla zdrowia człowieka.5
Nie tylko komórki odpornościowe: znaczenie jelitowej bariery sluzowej
Dr. Larissa Celiberto
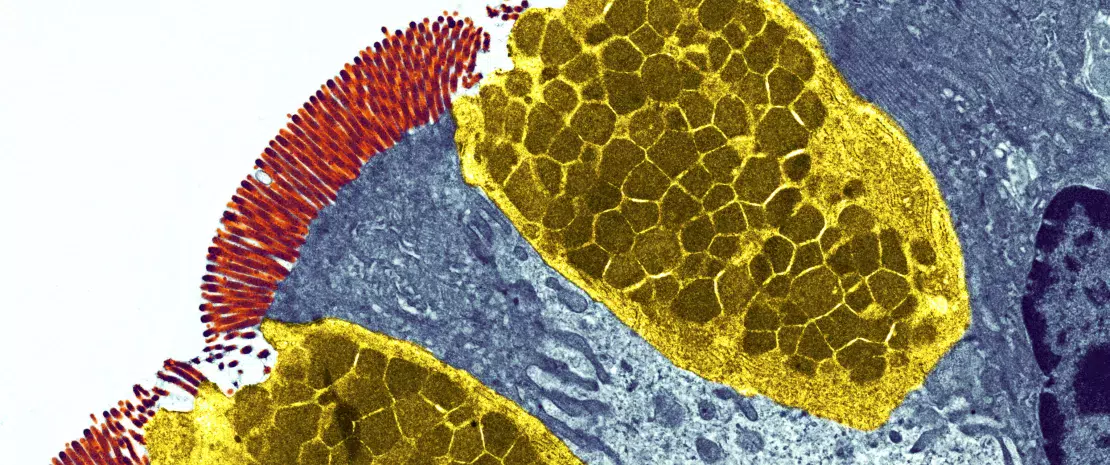
Jelito jest wyścielone pojedynczą warstwą komórek zwanych nabłonkiem jelitowym i pokrytych warstwą gęstego śluzu (rys. 1). Razem bariery te zatrzymują mikroorganizmy w świetle jelita, a także chronią układ odpornościowy przed niepotrzebnym pobudzaniem przez mikrobiotę.3 Śluz jelitowy wytwarza i uwalnia mucynę 2 (MUC2) – pokryta cukrem glikoproteinę nadającą śluzowi strukturę. Niedawne badania wykazały, że na dojrzewanie i funkcjonowanie powłoki śluzowej duży wpływ ma mikrobiota jelit, natomiast cukry znajdujące się na powierzchni MUC2 mogą również wpływać na to, które bakterie są zdolne do przywierania do niej lub wykorzystywania jej i jej łańcuchów cukrowych jako źródła pożywienia.7 Zwłaszcza przerwanie lub zaburzenie działania bariery śluzowej może prowadzić do zwiększonej penetracji lub przenikania potencjalnie szkodliwych bakterii ze światła (np. w przypadku zespołu nieszczelnego jelita), co powoduje ogólnoustrojową infekcję i stan zapalny.8 Co więcej, w przypadku kilku chorób zaobserwowano uszkodzenie powłoki śluzowej oraz związaną nim dysbiozę jelitowe9 (choroby te to np. nieswoiste zapalenia jelit (IBD),10,11 cukrzyca i p.12 ), co podkreśla znaczenie tej ochronnej bariery dla zdrowia człowieka..
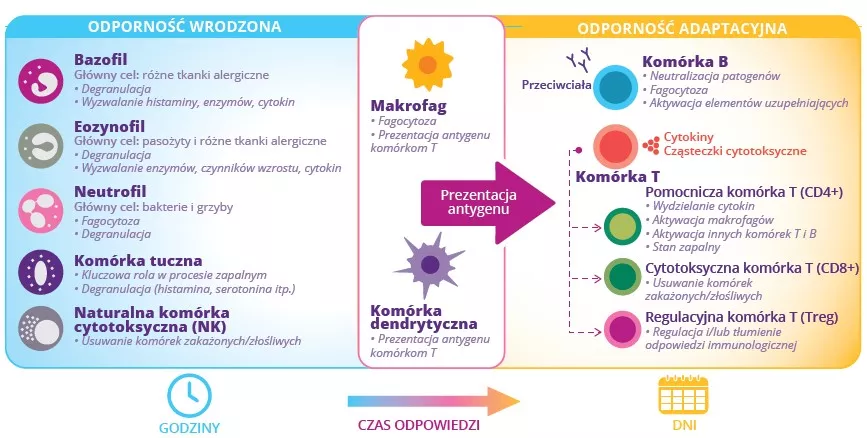
RYSUNEK 2: Komórki wrodzonych i adaptacyjnych systemów odpornosciowych oraz ich odpowiednie funkcje.
3 Brandtzaeg P. (2017) Role of the Intestinal Immune System in Health. In: Baumgart D. (eds) Crohn's Disease and Ulcerative Colitis. Springer, Cham.
4 Commins SP. Mechanisms of Oral Tolerance. Pediatr Clin North Am. 2015 Dec;62(6):1523-9.