A Microbiota Vaginal # 16
Pela Prof. Satu Pekkala
Investigador na Academia da Finlândia, Faculdade de Ciências do Desporto e da Saúde, Universidade de Jyväskylä, Finlândia



Pela Prof. Satu Pekkala
Investigador na Academia da Finlândia, Faculdade de Ciências do Desporto e da Saúde, Universidade de Jyväskylä, Finlândia

Todos os anos, são relatados quase 90 milhões de casos de gonorreia em todo o mundo. Nas mulheres, a infeção do trato genital inferior pela Neisseria gonorreia tem consequências altamente variáveis, desde a ausência de sintomas até à cervicite. Embora os fatores subjacentes a esta variabilidade não sejam conhecidos, a microbiota cervico-vaginal pode estar envolvida. De facto, uma equipa demonstrou recentemente que a microbiota cervico-vaginal prediz a apresentação clínica da gonorreia nas mulheres.
Estes são os resultados de um estudo piloto nos EUA sobre 19 pacientes infetados com N. gonorreia, 10 dos quais eram sintomáticos e 9 assintomáticos. A maioria destes pacientes eram afro-americanos, uma população cuja microbiota é mais frequentemente baixa em lactobacilos do que a das mulheres caucasianas. Neisseria spp. representava apenas 0,24% das bactérias presentes em todos os 19 pacientes, quer sintomáticos quer assintomáticos. Metade das pacientes de cada grupo também tiveram coinfecções com Chlamydia trachomatis e/ou Trichomonas vaginalis.
A microbiota cervico-vaginal dos pacientes assintomáticos sem coinfecção continha mais frequentemente comunidades microbianas dominadas por lactobacilos (92,2% de bactérias em média) do que a dos pacientes sintomáticos sem coinfecção (21,6%).
Em contraste, as mulheres sintomáticas tinham comunidades microbianas caracterizadas por taxas bacterianas mais diversas e heterogéneas. Eram compostas por uma mistura de bactérias anaeróbias associadas à vaginose bacteriana (BV): Prevotella, Sneathia, Mycoplasma hominis e Bacterial Vaginosis-Associated Bacterium- 1 (BVAB1) / Candidatus Lachnocurva vaginae.
Estes resultados são meramente os de um estudo piloto baseado numa pequena amostra. Este é um primeiro passo crucial, mas são necessários mais estudos para avaliar o efeito potencialmente protetor contra a infeção por N. gonorreiae de uma microbiota vaginal dominada por Lactobacillus.
Pela Prof. Satu Pekkala
Investigador na Academia da Finlândia, Faculdade de Ciências do Desporto e da Saúde, Universidade de Jyväskylä, Finlândia
Os inibidores do ponto de controlo imunitário (ICI) melhoraram significativamente o tratamento do melanoma avançado. No entanto, nem todos os pacientes respondem ao tratamento, que se pensa estar ligado à microbiota intestinal. Lee et al. realizaram a sequenciação metagenómica de amostras fecais de cinco coortes europeias de ICI, com um total de 165 pacientes com melanoma cutâneo avançado. Devido a diferenças clínicas e mutacionais entre as coortes, foram analisados separadamente e não agrupados. Os autores encontraram uma diferença significativa na composição da microbiota intestinal entre respondedores e não respondedores na coorte PRIMM-UK, mas não na coorte PRIMM-Netherland (NL). Além disso, ao analisar as bases de dados disponíveis publicamente (n = 147 amostras metagenómicas), tornou-se evidente que havia uma reprodutibilidade limitada das previsões de resposta entre as coortes. Nenhuma bactéria era um biomarcador inteiramente constante de resposta aos ICI em todos os conjuntos de dados. No entanto, um painel de espécies microbianas, incluindo Bifidobacterium pseudocatenulatum, Roseburia spp. e Akkermansia muciniphila, foi identificado no estudo associado com os respondedores. Quanto aos genes funcionais da microbiota, por exemplo, as adeninas metílases de ADN foram aumentadas nos respondedores. Em conclusão, embora tenha sido identificado um potencial painel de biomarcadores microbianos mostrando a capacidade de resposta ao tratamento ICI, são necessários estudos futuros em coortes maiores. Além disso, vários fatores clínicos devem ser considerados como confusos ao avaliar os biomarcadores que podem ser úteis no diagnóstico.
de células não pequenas (NSCLC) não respondem ao tratamento com inibidores do ponto de controlo imunitário (ICI), tais como anti-PD-1. Provas recentes mostram que certos membros da microbiota intestinal, especialmente Akkermansia muciniphila, podem influenciar a eficácia dos ICI em pacientes com NSCLC. Além disso, a resistência ao tratamento tem sido associada a um microambiente tumoral inflamatório inferior. Derosa et al. estudo prospetivo e multicêntrico incluiu 338 pacientes com NSCLC avançados tratados com ICI para determinar se os perfis metagenómicos da microbiota intestinal poderiam explicar a resposta ao tratamento. Mostram que uma maior abundância de Akkermansia nas fezes de base estava associada a uma maior taxa de resposta ao tratamento com ICI, associada a um benefício clínico (aumento da sobrevida). Além disso, a presença de Akkermansia associada a outras mudanças potencialmente relevantes em termos de prognóstico na microbiota intestinal. Vários genes tumorais expressos de forma diferente foram ligados à resposta ao bloqueio PD-1 sugerindo que a Akkermansia poderia promover a migração de células T helper para o microambiente tumoral. Para finalmente mostrar que a Akkermansia podia salvar a resistência ao ICI, os autores inocularam duas estirpes diferentes de A. muciniphila em ratos que foram previamente transplantados com fezes de um paciente com resistência ao bloqueio PD-1. Em comparação com os ratos de controlo, as duas estirpes resgataram a resposta ao tratamento. De longe, este estudo é a maior análise prospetiva metagenómica que validou a Akkermansia como um potencial fator prognóstico para os pacientes tratados com NSCLC com ICI e mostrou o potencial mecanicista da Akkermansia.
A única indicação validada para o FMT é a infeção recorrente por Clostridioides difficile. Contudo, o envolvimento da microbiota intestinal em numerosas outras doenças (doença de Parkinson, por exemplo) sugere que as indicações para FMT poderiam em breve ser expandidas. A microbiota intestinal também pode modificar numerosos processos associados à depressão, tais como o eixo hipotálamo-hipófise-adrenal da glândula. Até agora, não existem ensaios publicados que utilizem o FMT para tratar pacientes com condições bipolares. O estudo longitudinal de Parker et al. apresenta o caso de um homem de 28 anos de idade com doença bipolar. Aos 10 anos de idade, desenvolveu episódios depressivos. Os sintomas incluíam um humor severamente deprimido, pensamentos suicidas, anergia, concentração reduzida, retardamento psicomotor e insónia. Os sintomas eram geralmente associados à irritabilidade e ansiedade. Aos 15 anos de idade, desenvolveu o seu primeiro episódio hipomaníaco. Durante anos, foi tratado com sucesso com drogas, mas depois voltaram a ocorrer problemas de humor. Começou voluntariamente a tomar probióticos (estirpes de Lactobacillus e Saccharomyces. Depois dos probióticos, ele próprio relatou um enorme alívio dos sintomas. Encorajado pelas melhorias, o paciente leu sobre a investigação microbiológica e optou por experimentar o FMT. Este procedimento foi realizado através de colonoscopia por um gastroenterologista. Após o FMT, ele traçou os seus estados de humor durante 470 dias consecutivos. Ele auto-relatou que os episódios de humor diminuíram em frequência e severidade ao longo dos meses. Foi também capaz de reduzir significativamente o tratamento medicamentoso. Doze meses após o FMT, declarou ter tido níveis elevados distintos, praticamente sem sintomas bipolares, e os sintomas do distúrbio de hiperatividade de défice de atenção tinham melhorado. Embora este seja apenas um estudo de caso, o FMT foi capaz de reduzir os sintomas bipolares, justificando assim a necessidade de estudos FMT em coortes bipolares maiores.
FEEDBACK DE CONGRESSOS
Pelo Prof. Koen Huysentruyt
Gastrenterologia, hepatologia e nutrição pediátricas, Centro de Reabilitação Intestinal Infantil de Bruxelas (BCIRC), Bélgica

A 54.a reunião ESPGHAN anual teve lugar de 22 a 25 de junho de 2022 na bela cidade de Copenhaga. Foi a primeira vez que a reunião se realizou de novo na vida real, após dois anos de limitações devido à pandemia de Covid. Foi uma grande oportunidade para se encontrar com especialistas em gastroenterologia, hepatologia e nutrição pediátricas de todo o mundo para partilhar conhecimentos, investigação e novas perspetivas interessantes. O objetivo deste artigo é destacar alguns dos tópicos abordados sobre o microbioma.
Prof. Dennis Sandris Nielsen apresentou- nos o viroma, uma coleção de vírus que transportamos, que é um campo de investigação emergente que parece desempenhar um papel importante na saúde humana e na doença. A análise da amostra fecal mostra que aproximadamente 6% do ADN encontrado não é de origem bacteriana, mas de origem viral. Por cada bactéria no corpo humano, um vírus corresponde a ela. Tal como o microbioma, o viroma é influenciado por fatores pré, peri e pós-natais (dieta, ambiente, irmãos, medicamentos, etc.). Estes vírus são assim omnipresentes no intestino e desempenham um papel fundamental na regulação do microbioma intestinal. Os bacteriófagos são um tipo de vírus que atacam bactérias numa matéria específica do hospedeiro. São descritos dois tipos diferentes de interações: a “kill-the-winner dynamics” e a “piggyback-the-winner dynamics”. No primeiro, os bacteriófagos atacam as bactérias, injetam o seu ADN e utilizam as bactérias como hospedeiro para criar novas partículas de fago depois de a célula ser lisada. O orador faz uma analogia com os leões e as gazelas na Savana, significando uma dinâmica de constante diversidade, destruição dos concorrentes de nicho, desvio de fago e rotação bacteriana e pressão sobre o hospedeiro para diversificação do recetor de fago. No último, o vírus cavalga com o vencedor, integrando o seu ADN no genoma da bactéria, alterando a célula hospedeira e tornando-a mais eficiente, tornando assim o vencedor num vencedor. Um estudo sobre amostras fecais de uma população infantil saudável na Dinamarca identificou mais de 10.000 espécies virais, pertencentes a 248 famílias virais. Notavelmente, 232 dessas famílias não foram descritas anteriormente, apoiando a hipótese de que apenas a ponta do iceberg foi ainda descoberta [1]. As questões que são levantadas são que implicações tem na saúde humana, e se desempenha um papel no amadurecimento do sistema imunitário. O desequilíbrio viromático intestinal pode desempenhar um papel no desenvolvimento da doença (ou seja, VEO-IBD, NEC, etc.).
O modo de parto à nascença desempenha um papel fundamental na formação precoce do microbioma intestinal. Os bebés que nascem por via vaginal são expostos a diferentes estirpes bacterianas em comparação com os que nascem por cesariana, com uma colonização diferente como consequência. Além disso, a razão para uma cesariana é na maioria das vezes devida a uma emergência fetal. Esses bebés são mais propensos a ter um pH baixo no sangue do cordão umbilical, o que causa uma redução na permeabilidade da junção apertada promovendo a disbiose.
A amamentação parece neutralizar o efeito pernicioso da cesariana na microbiota e continua a ser o padrão dourado na nutrição infantil. No entanto, as mulheres que dão à luz por cesariana têm menos probabilidades de amamentar, ou atrasam a iniciação da amamentação, e os bebés são então alimentados com leite em pó. Por esta razão, os investigadores procuram constantemente o cocktail perfeito de pré, pró, sin ou pós-bióticos para imitar o microbioma intestinal de um bebé amamentado.
O Dr. Eduardo López-Huertas discutiu uma estirpe de Lactobacillus. fermentum e mostrou resultados promissores em bebés nascidos por cesariana. Num ensaio aleatorizado controlado (RCT), analisaram as amostras de fezes de bebés alimentados com um leite em pó simbiótico contendo L. fermentum e GOS e encontraram grandes semelhanças com as amostras de bebés amamentados (bifidobactérias superiores, pH fecal inferior) [2]. Além disso, é demonstrado numa meta-análise recente (3 ensaios) que L. fermentum reduz a incidência de infeções gastrointestinais com 73% em bebés nascidos por cesariana. É necessária mais investigação para investigar possíveis vantagens na prevenção de potenciais doenças, ou seja, infeções do trato gastrointestinal ou do trato respiratório, especialmente em bebés nascidos por cesariana, que têm um microbioma intestinal desvantajoso [3].
O Dr. Giles Major forneceu-nos os seus conhecimentos sobre a ligação entre os glicanos e o microbioma intestinal. Os glicanos ou oligossacarídeos do leite humano (HMO) afetam a composição geral do microbioma intestinal. O leite materno é composto por muitos HMO diferentes que variam em concentração no leite materno, dependendo da etnia da mãe e durante o crescimento do bebé. Quando o microbioma intestinal é investigado numa idade precoce, notamos uma predominância de bifidobactérias no leite materno em comparação com os lactentes alimentados com leite em pó. Estas bifidobactérias são importantes porque absorvem carbono e produzem ácidos gordos de cadeia curta que modulam a permeabilidade da barreira intestinal. A sua fonte de carbono são HMO, e o microbioma desempenha um papel na digestão desses HMO através da presença de CAZymes. Assim, os CAZymes que tiver, determinarão quais os glicanos que pode digerir e o tipo de glicanos que uma criança é alimentada conduzirá a maturação do microbioma nos primeiros anos de vida.
Foi realizado um RCT no qual um grupo de controlo de bebés alimentados com leite em pó foi comparado a grupos de teste que receberam um leite em pó 5-HMOBlend. O ensaio ainda está em curso, mas os resultados preliminares mostram que a diversidade microbiana intestinal global foi significativamente diferente no grupo de controlo em comparação com o grupo de ensaio, sendo que no grupo de teste a composição se tornou mais semelhante à dos bebés amamentados. O orador sugere que isto poderia ser a consequência da promoção de bifidobactérias, embora isto tenha sido apenas uma especulação.
Artigo comentado - rubrica pediátrica
Pelo Prof. Emmanuel Mas
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França

O microbioma intestinal nos primeiros anos de vida desempenha um papel crítico no desenvolvimento do hospedeiro e influencia o funcionamento do cérebro. Este estudo investigou a associação entre a sucessão do microbioma intestinal desde a primeira semana de vida e o crescimento da circunferência da cabeça (HCG). Foram recolhidas semanalmente amostras de fezes de uma coorte de recémnascidos pré-termo, a fim de avaliar a composição microbiana intestinal, em conjunto com dados clínicos e medições da circunferência da cabeça. Os bebés prematuros com trajetórias subótimas de HCG tiveram um esgotamento na abundância/prevalência de Bacteroidota e Lachnospiraceae, que não estava relacionado com a morbilidade e restrição calórica. Este artigo fornece provas de que a sua integração no microbioma intestinal precisa de ocorrer precocemente para um desenvolvimento neurológico ótimo.
As perturbações do desenvolvimento neurológico são frequentes em crianças pequenas, afetando até 8,4% dos indivíduos com menos de 5 anos de idade em todo o mundo. O crescimento da circunferência da cabeça (HCG) é um marcador correlacionado com o neurodesenvolvimento precoce.
É importante procurar fatores ambientais que possam ser modificados para reduzir as perturbações do desenvolvimento neurológico. Os estudos de nutrição interventiva não demonstraram resultados significativos no neurodesenvolvimento (por exemplo: o benefício do aleitamento materno). Os autores investigaram o microbioma intestinal (GM) porque a sua aquisição durante os primeiros meses de vida e o uso de antibióticos durante o primeiro ano estão associados a várias patologias, incluindo as perturbações do neurodesenvolvimento mais tarde na infância, em particular a perturbação do défice de atenção e a perturbação do espectro do autismo. O objetivo do estudo era determinar se existe uma relação entre as características do GM inicial e uma trajetória subótima do HCG (SHCGT).
Os bebés com < 37 semanas de idade pós-menstrual (unidade de cuidados neonatais de Chicago) foram incluídos entre janeiro de 2010 e dezembro de 2018. A trajetória do HCG foi a diferença entre os z-scores da circunferência da cabeça medidos à nascença e às 36 semanas pós-menstrual (PMA); foram utilizadas perdas de 0,5 z-scores de intervalo para definir os grupos com uma trajetória adequada de HCG (AHCGT) ou uma trajetória subótima (ligeiramente, moderada e severamente prejudicada, SHCGT).
A β-diversidade do GM diferiu significativamente entre os bebés SHCGT e AHCGT, assim como a alteração da abundância dos taxa nas amostras de fezes a 30 PMA. A perda em HCG z- score > 0,5 ocorreu entre 31 e 36 semanas PMA nos grupos SHCGT. Isto sugere que um GM “imaturo” precede o SHCGT.
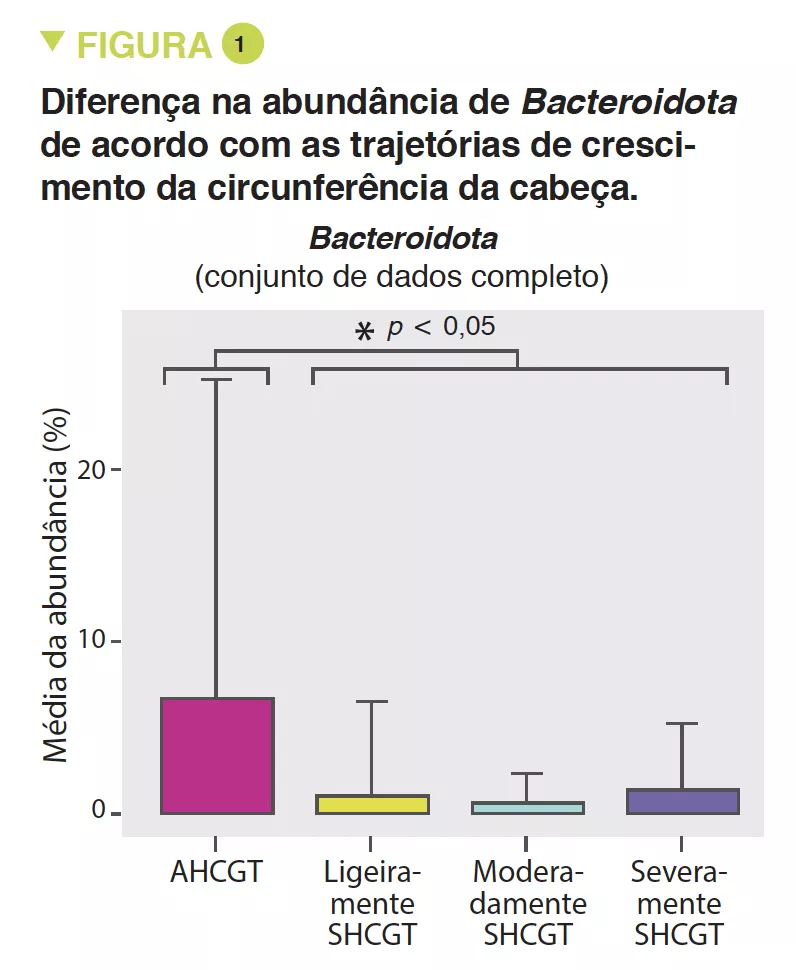
SHCGT infants had a significantly decreased abundance of Bacteroidota (p = 0.0009) (Figure 1) and Lachnospiraceae (p = 0.009), between 31 and 36 weeks PMA, which may result in a reduced carbohydrate utilisation capacity of these taxa. The prevalence of the Ruminococcaceae family (p = 0.007) was attributed to the species Faecalibacterium prausnitzii (p = 0.004), 48% in the AHCGT vs 8% in the SHCGT infants. It is to be noted that there was an increase in Firmicutes in the SHCGT groups from 24 to 30 weeks PMA (p = 0.009) but without any difference in the sub-taxa.
Os bebés SHCGT tiveram uma diminuição significativa da abundância de Bacteroidota (p = 0,0009) (Figura 1) e Lachnospiraceae (p = 0,009), entre 31 e 36 semanas de PMA, o que pode resultar numa redução da capacidade de utilização de hidratos de carbono destes taxa. A prevalência da família Ruminococcaceae (p = 0,007) foi atribuída à espécie Faecalibacterium prausnitzii (p = 0,004), 48% no AHCGT vs 8% nos bebés SHCGT. É de notar que houve um aumento de Firmicutes nos grupos SHCGT de 24 para 30 semanas PMA (p = 0,009) mas sem qualquer diferença na sub-taxa.
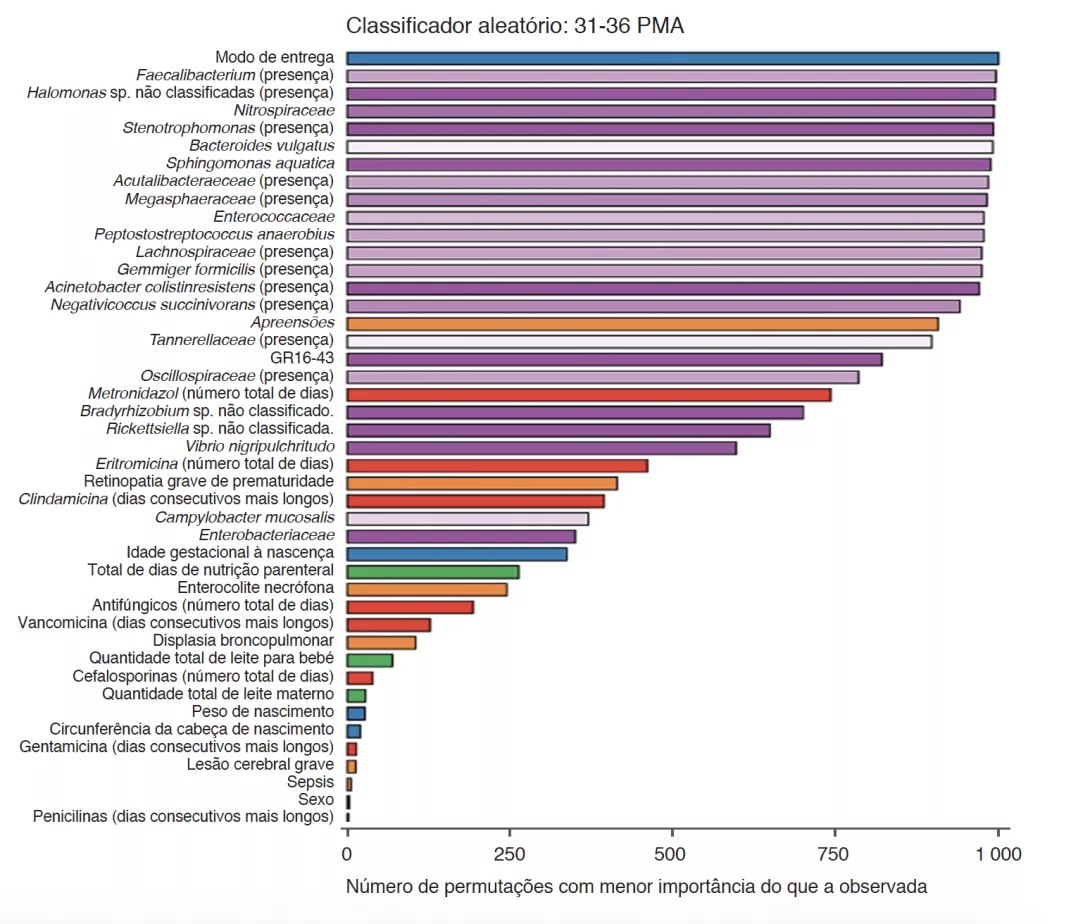
A análise dos parâmetros clínicos mostrou que as alterações no HCG não se deviam a restrições calóricas. Houve mais morbilidades nas crianças dos grupos SHCGT do que naquelas com AHCGT: enterocolite necrosante (p = 0,0006), lesão neurológica grave (p = 0,01), sepsis (p = 0,03). Contudo, os métodos analíticos utilizados, tais como a decisão aleatória com permutações, mostraram que os fatores mais importantes associados às trajetórias do HCG foram as características do GM e não as comorbilidades, quer de 24 a 30 PMA ou de 31 a 36 PMA (Figura 2). Em bebés livres de morbilidades graves, as diferenças em Bacteroidota e Lachnospiraceae ainda estavam presentes, mas a abundância de Actinobacteriota foi significativamente maior no grupo AHCGT e no grupo SHCGT ligeiro do que nos grupos moderada e severamente SHCGT. O tipo de parto teve mais efeito nas trajetórias de HCG do que fatores que influenciam o GM, tais como nutrição entérica e tratamentos com antibióticos. Isto está ligado à transmissão do GM no parto porque a abundância de Bacteroidota foi maior em bebés por parto vaginal do que naqueles com parto por cesariana. Além disso, entre os bebés por parto vaginal, aqueles com um SHCGT tiveram uma queda na abundância dos taxa acima descritos como relacionados com as trajetórias do HCG, em comparação com o AHCGT. Além disso, o termo de nascimento é um fator importante porque todos os bebés SHCGT por parto vaginal nasceram < 27 semanas de idade pós-menstrual, enquanto apenas 17% dos bebés AHCGT por parto vaginal nasceram < 27 semanas de idade pós menstrual.

Sugere-se, portanto, que SHCGT começa com uma redução da abundância de Bacteroidota e Lachnospiraceae, e depois é exacerbado com a redução em Actinobacteriota.
O nascimento por via vaginal permite a transmissão vertical de Bacteroidota.
Deve-se, no entanto, estar vigilante em relação aos bebés nascidos antes das 27 semanas de PMA, porque mesmo aqueles que nascem por via vaginal parecem estar em maior risco de SHCGT.
O microbioma intestinal é um fator importante que influencia a trajetória de crescimento da circunferência da cabeça. A aquisição muito precoce de certas bactérias (Bacteroidota e Lachnospiraceae), potenciada por um parto vaginal, pode reduzir as perturbações de desenvolvimento neurológico.
ARTIGO COMENTADO - FASE ADULTA
Pelo Prof. Pr Harry Sokol
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França

A microbiota fúngica (micobiota) é parte integrante da complexa comunidade microbiana que coloniza o trato gastrointestinal dos mamíferos e tem um papel importante na regulação imunitária. Embora as alterações na micobiota tenham sido associadas a várias doenças, incluindo a doença inflamatória intestinal (DII), desconhece-se atualmente se as espécies fúngicas identificadas por sequenciação representam organismos vivos e se fungos espec íficos têm efeitos sobre o desenvolvimento da DII. Os autores desenvolveram uma plataforma translacional para a análise funcional do micobioma. Combinando sequenciação micobiótica de alta resolução, culturomia fúngica e genómica, um sistema de edição de estirpes fúngicas baseado no CRISPR-Cas9, ensaios de imunorreatividade funcional in vitro e modelos in vivo, esta plataforma permite o exame do diafragma do hospedeiro-fungo no intestino humano. Descobrimos uma rica diversidade genética de estirpes oportunistas de Candida albicans que dominam a mucosa cólica de pacientes com DII. Entre estas estirpes isoladas, as estirpes com elevada capacidade de destruição das células imunitárias (estirpes HD) refletem as características da doença de pacientes com colit e ulcerosa e agravam a inflamação intestinal in vivo através de mecanismos dependentes da IL-1β. As respostas inflamatórias e antifúngicas das células T auxiliares produtoras de interleucina-17A (células Th17) induzidas pelas estirpes HD no intestino estavam dependentes da candialíssima, a toxina peptídea segregada pela C. albicans durante a transição de um estado comensal benigno para um estado patogénico. Estas descobertas revelam a natureza específica da estirpe das interacções hospedeiro-fúngicas no intestino humano e destacam novos alvos de diagnóstico e terapêuticos para a DII.
Estudos baseados no sequenciamento profundo da micobiota intestinal em várias coortes de pacientes fornecem provas coerentes de que a “disbiose fúngica” é uma característica da doença inflamatória crónica intestinal (DII) [2], cujas formas mais disseminadas são a doença de Crohn (DC) e a colite ulcerativa (CU), que afetam milhões de indivíduos em todo o mundo. Os anticorpos anti-Saccharomyces cerevisiae (ASCA), dirigidos contra os mananos apresentados pela parede celular dos fungos, definem subtipos de DII, porque a sua presença no soro está associada à DC mas não à CU, o que estabelece uma ligação adicional entre os fungos e a DII. Candida é o género fúngico mais difundido, e a sua presença é sistematicamente aumentada em várias coortes de pacientes com DII analisados por sequenciação da microbiota fecal [2].
Em particular, a C. albicans no intestino induz um conjunto de anticorpos antifúngicos e atua como imunogéneo para ASCA. As espécies de Candida associadas à mucosa intestinal são detetadas pelos macrófagos presentes no intestino e demonstraram experimentalmente ter o potencial de induzir imunidade protetora ou de desencadear inflamação, dependendo do contexto [3]. Apesar desta evidência, desconhece-se atualmente se os fungos detetados por tecnologias de sequenciação no intestino humano têm um papel essencial na orientação da imunidade da mucosa ou na evolução da doença inflamatória em cada paciente individual. Tem-se observado repetidamente uma falta de correlação entre as alterações na composição da micobiota e a gravidade da doença nas coortes de pacientes com DII, apesar de um aumento constante das espécies de Candida. Os autores emitiram assim a hipótese de que a diversidade funcional das estirpes de Candida determina a relação hospedeiro-fungo na mucosa intestinal humana com um efeito na inflamação intestinal.
De acordo com numerosos outros estudos, os autores observaram pela primeira vez que as micobiota dos pacientes com UC eram ricas em Candida albicans e, em contraste, pobres em Saccharomyces. Na situação de resposta imunitária prejudicada induzida pela terapia com corticosteroides, a C. albicans exacerba a gravidade da colite em ratos. Os autores isolaram então várias estirpes de C. albicans da micobiota de sujeitos saudáveis e de pacientes com UC e observaram uma grande heterogeneidade em termos de capacidade pró-inflamatória. Em particular, a capacidade de causar danos celulares aos macrófagos, que são uma defesa fundamental contra os fungos, varia de uma estirpe para outra. As estirpes capazes de infligir danos celulares aos macrófagos têm uma maior tendência para o filamento e têm efeitos pró-inflamatórios in vivo, induzindo uma resposta Th17 (Figura 1).Os autores mostraram então que grande parte dos efeitos próinflamatórios foram mediados pela secreção de uma toxina, candialíssima, e pela indução da produção de IL-1β. As análises subsequentes revelaram uma forte correlação entre a capacidade pró-inflamatória de estirpes isoladas de pacientes com UC e a atividade inflamatória da doença. Por outro lado, não houve correlação entre a magnitude da inflamação intestinal e a abundância global de Candida albicans nos pacientes. Estes resultados explicam a fraca correlação entre a composição da micobiota e as características das patologias humanas e sugerem que as capacidades funcionais (pró-inflamatórias, neste caso) podem fornecer uma melhor explicação do papel da micobiota nestas patologias.
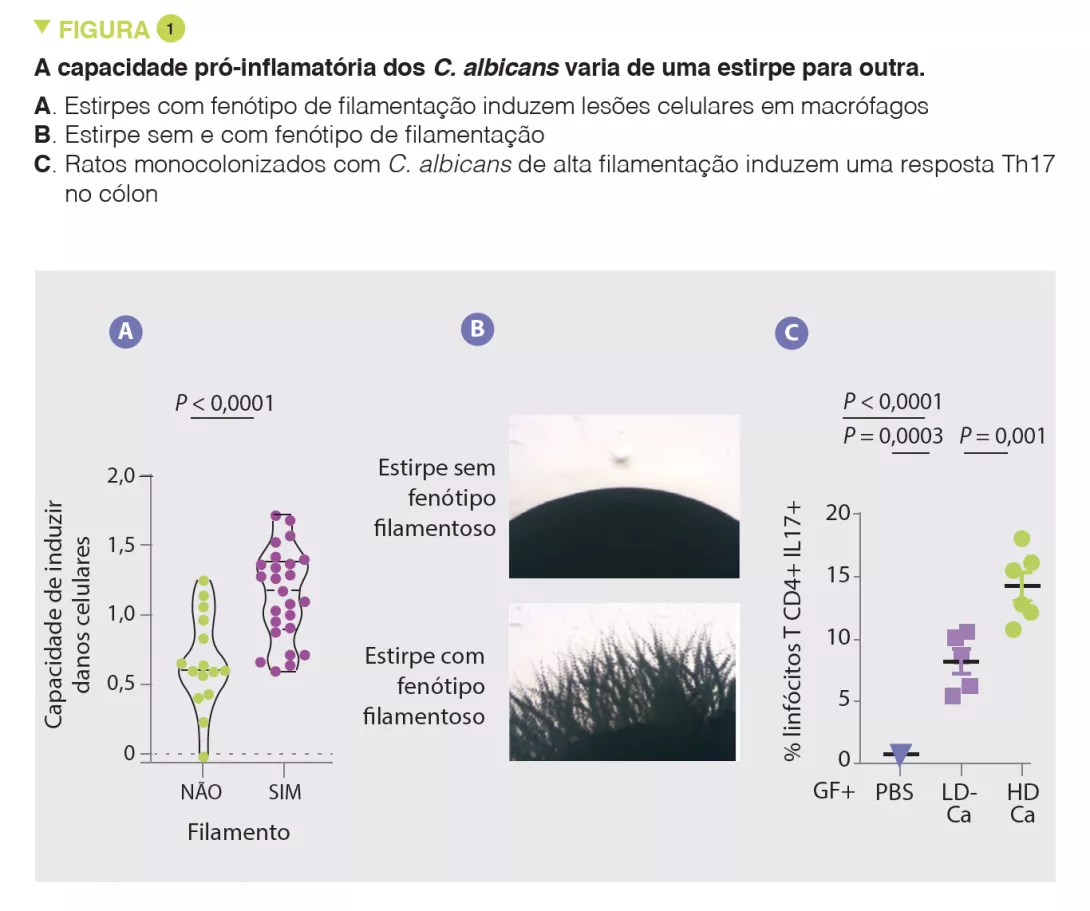
Este estudo mostra que, para além das análises da composição da micobiota, em particular através da sequenciação, é necessária uma análise funcional para compreender a sua contribuição para a doença e, em particular, no DII. Se se confirmar que as estirpes pró-inflamatórias de C. albicans, candidalisina e IL-1β têm um papel na UC, podemos imaginar uma opção terapêutica que visa um destes elementos, especialmente porque já estão disponíveis várias moléculas que antagonizam a via da IL-1β.
Este estudo sugere que a candialíssima é um fator chave no efeito pró-inflamatório de C. albicans no intestino e que algumas estirpes altamente pró-inflamatórias atuam através de mecanismos dependentes de IL-1β. Os pacientes portadores de estirpes altamente pró-inflamatórias podem representar uma população alvo para um tratamento antagonista da IL-1β e/ou da C. albicans.
1. Li XV, Leonardi I, Putzel GG, et al. Immune regulation by fungal strain diversity in inflammatory bowel disease. Nature 2022 ; 603 : 672-8.
2. Sokol H, Leducq V, Aschard H, et al. Fungal microbiota dysbiosis in IBD. Gut 2017 ; 66 : 1039-48.
3. Doron I, Leonardi I, Li XV, et al. Human gut mycobiota tune immunity via CARD9-dependent induction of anti-fungal IgG antibodies. Cell 2021 ; 184 : 1017-1031.e14.
Síntese
Pelo Dr. Jay Patel
Usher Institute of Population Health Sciences and Informatics, Universidade de Edimburgo, Reino Unido

A boca acomoda uma elevada e diversificada carga bacteriana incorporada dentro de matrizes extracelulares. A má higiene oral encoraja mudanças disbióticas nestes biofilmes polimicrobianos, fomentando a colonização e proliferação de espécies bacterianas cada vez mais patogénicas. Embora se saiba que a microbiota medeia a inflamação, estudos recentes sugerem que a disbiose da microbiota oral pode estar associada à gravidade e duração dos sintomas da Covid-19. Para estes pacientes, manter ou melhorar as práticas de higiene oral pode melhorar os resultados clínicos.
As infeções virais são conhecidas por precipitar as coinfecções bacterianas. A maioria das mortes na pandemia de gripe de 1918 foi diretamente atribuível a pneumonia bacteriana secundária [1]. Além disso, resultados clínicos graves durante a pandemia de gripe H1N1 de 2009 foram associados a coinfecções bacterianas [2]. O desafio da copatogénese bacteriana viral durante os surtos de doenças infecciosas pode complicar significativamente a resposta global, retardar a recuperação, e acelerar a resistência antimicrobiana. Felizmente, os resultados de um estudo de coorte multicêntrico de quase 50.000 pacientes revelaram que poucas infeções bacterianas foram relatadas em pacientes hospitalizados com Covid-19 [3]. No entanto, é de notar que o diagnóstico de coinfecções é complexo, pois os organismos podem apresentar-se antes da infeção viral; como parte de uma infeção crónica subjacente; ou podem ser contraídos nosocomialmente [4].
A cavidade oral e as vias respiratórias superiores abrigam uma carga bacteriana elevada e ricamente diversificada. Na saúde, o microbioma oral mantém uma relação harmoniosa e bem afinada, mas pequenas mudanças nos comportamentos de rotina podem causar mudanças ecológicas substanciais nesta simbiose. Uma higiene oral deficiente pode tornar o ambiente patogénico, transformando o microbioma num estado de disbiose, onde as condições dos processos da doença são melhoradas [5, 6].
A doença periodontal - inflamação crónica da gengiva (gengiva) - é principalmente mediada pelos componentes inflamatórios dentro do biofilme e altera a arquitectura dos tecidos gengivais para apresentar micro- úlceras. Estes formam uma comunicação entre a cavidade oral e o sangue, que leva a atividades de rotina (por exemplo, mastigação, fio dental e escovagem dos dentes) induzindo a bacteremia. As bactérias orais e os mediadores inflamatórios são então amplamente disseminados através do sangue, atingindo os sistemas de órgãos vitais. As provas mostram que a exposição à bacteremia pode ser significativamente prejudicial e contribuir para uma inflamação sistémica de baixo grau que precipita condições inflamatórias [5]. Além disso, sabe-se que a periodontite é um fator agravante na incidência de diabetes tipo II e que a microbiota disbiose oral está envolvida tanto em perturbações periodontais como metabólicas (doenças cardiovasculares, dislipidemia...) [7].
A investigação sobre esta associação é limitada, mas os poucos estudos que existem apontam para ligações intrigantes. Um estudo transversal duplo-cego de 303 pacientes Covid-19 confirmados por PCR no Egipto investigou a interação entre três fatores: 1) a higiene oral; 2) a gravidade da Covid-19; e 3) os valores da proteína C-reativa (CRP). A CRP é um marcador de hiper-inflamação, pelo que os pacientes com níveis elevados de CRP foram colocados na hipótese de terem um prognóstico mais pobre com a COVID-19 [8]. Os investigadores descobriram que a saúde oral deficiente estava correlacionada com o aumento dos valores de CRP e o atraso do período de recuperação.
Um estudo de controlo de casos (inigualável) de 568 pacientes no Qatar revelou que a periodontite estava associada a complicações graves da COVID-19, incluindo um aumento de 3,5 vezes na necessidade de um ventilador; um aumento de 4,5 vezes no risco de admissão em cuidados intensivos; e um aumento de 8,8 vezes no risco de morte [9]. Embora estes resultados não sugiram a causalidade e outros fatores possam estar implicados, as associações são duras e justificam mais perguntas sobre o verdadeiro papel da disbiose oral nos resultados da Covid-19.
Esta relação em grande parte hipotética baseia-se numa série de fatores que têm relevância comum na fisiopatologia da infeção pelo SARS-CoV-2 e periodontite. Por exemplo, a evidência radiológica pulmonar de processos patológicos vasculares primários sugere um eixo oral-vascular- pulmonar formando uma via direta de infeção, para além da entrega vascular direta aos vasos pulmonares (Figura 1) [10]. Em segundo lugar, as análises metagenómicas determinaram que o trato respiratório superior - um local anatómico inicial chave de infeção - é elevado em espécies bacterianas implicadas em doenças orais, e o papel da cavidade oral como um reservatório viral natural. Em terceiro lugar, a sobrevivência viral adequada dentro do biofilme sub-gengival e a capacidade de translocação viral da saliva para a bolsa periodontal - ambos contribuindo para uma evasão da resposta imunitária do hospedeiro. Em quarto lugar, a abundância de recetores da enzima de conversão da angiotensina 2 em componentes chave do eixo oral-vascular-pulmonar.
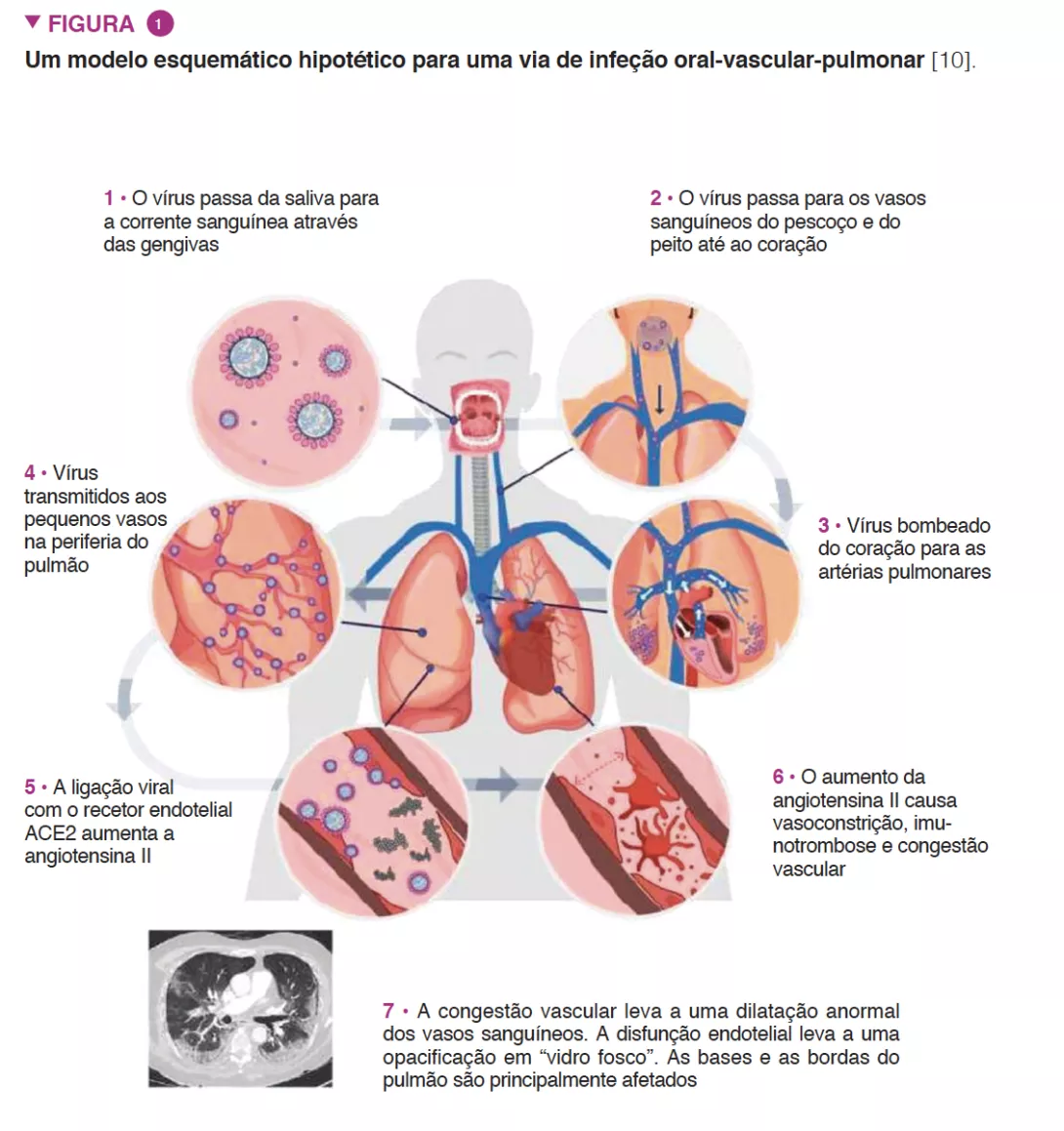
Independentemente da natureza precisa dos microrganismos orais implicados na fisiopatologia da Covid-19, uma boa higiene oral deve ser encorajada para os benefícios conhecidos para a saúde oral e geral. Escovação dentária escrupulosa duas vezes por dia, limpeza interdentária e utilização de um adjuvante de lavagem bucal são medidas relativamente simples que irão perturbar o biofilme, manter uma flora simbiótica e diminuir a concentração viral salivar.
Em resumo, o papel da má higiene oral na severidade dos resultados da Covid-19 é pouco estudado e pouco claro. No entanto, o papel potencial para uma interação clinicamente relevante segue-se logicamente. Manter ou melhorar as práticas de higiene oral tem claros benefícios para a saúde oral e geral e durante as infeções do SARS-CoV-2 pode também melhorar o prognóstico da doença.
Síntese
Pela Prof. Sian M. J. Hemmings
Departamento de Psiquiatria, Faculdade de Medicina e Ciências da Saúde, Universidade de Stellenbosch, Tygerberg, África do Sul

As perturbações relacionadas com o stress, incluindo as perturbações de stress pós-traumático (PSPT), as perturbações de ansiedade e as principais perturbações depressivas (MDD), são perturbações psiquiátricas comuns com uma resposta disfuncional ao stress um mecanismo patogénico chave. Estas perturbações são altamente complexas e debilitantes, estão associadas a um aumento da mortalidade e morbilidade. Existem provas consideráveis que implicam o papel da microbiota intestinal nas perturbações psiquiátricas, incluindo as perturbações relacionadas com o stress. Delinear um perfil microbiano intestinal específico associado ao desenvolvimento de perturbações psiquiátricas pode facilitar a identificação de biomarcadores fiáveis de risco associado à doença e prever a predisposição para desenvolver tais perturbações. Além disso, a microbiota intestinal pode ser facilmente manipulada e pode, portanto, oferecer uma opção de tratamento simples e sustentável para aliviar os sintomas das perturbações relacionadas com o stress. Este artigo analisa a literatura atual sobre o eixo microbioma-intestino-cérebro, e como este sistema bidirecional de comunicação pode desempenhar um papel na etiologia do PSPT, MDD e distúrbios de ansiedade.
As perturbações psiquiátricas são perturbações crónicas e debilitantes que prejudicam significativamente o funcionamento diário, e estão entre as dez principais causas de carga da doença a nível mundial [1]. A exposição a fatores de stress e trauma ambientais está associada ao aumento da incidência de transtorno de stress pós-traumático (PSPT), transtorno depressivo importante (MDD) e transtornos de ansiedade [2, 3]. Estas perturbações relacionadas com o stress estão associadas ao aumento da mortalidade, à redução da esperança de vida, são altamente comórbidas, e apresentam uma resposta variável à farmacoterapia de primeira linha. Não existem biomarcadores clinicamente acionáveis para estas perturbações, complicando ainda mais o seu diagnóstico e tratamento. Para facilitar o desenvolvimento de novas estratégias terapêuticas e potenciais intervenções, é imperativo que obtenhamos uma visão mais profunda dos mecanismos biológicos subjacentes a estas perturbações.
“Microbiota” é o termo que se refere aos triliões de microrganismos que vivem dentro e sobre nós. O catálogo completo destes microrganismos e dos seus genes constitui o microbioma humano. O microbioma intestinal, crucial na manutenção de numerosos aspetos do nosso funcionamento fisiológico, é um sistema dinâmico, cuja composição é afetada por numerosos fatores, incluindo a genética do hospedeiro, idade, dieta e etnia [4-6]. O eixo microbioma-intestino-cérebro (MGB) é um sistema complexo e bidirecional de comunicação entre o microbioma intestinal, o intestino, e o sistema nervoso central (SNC), facilitado por vias de comunicação diretas e indiretas (Figura 1).
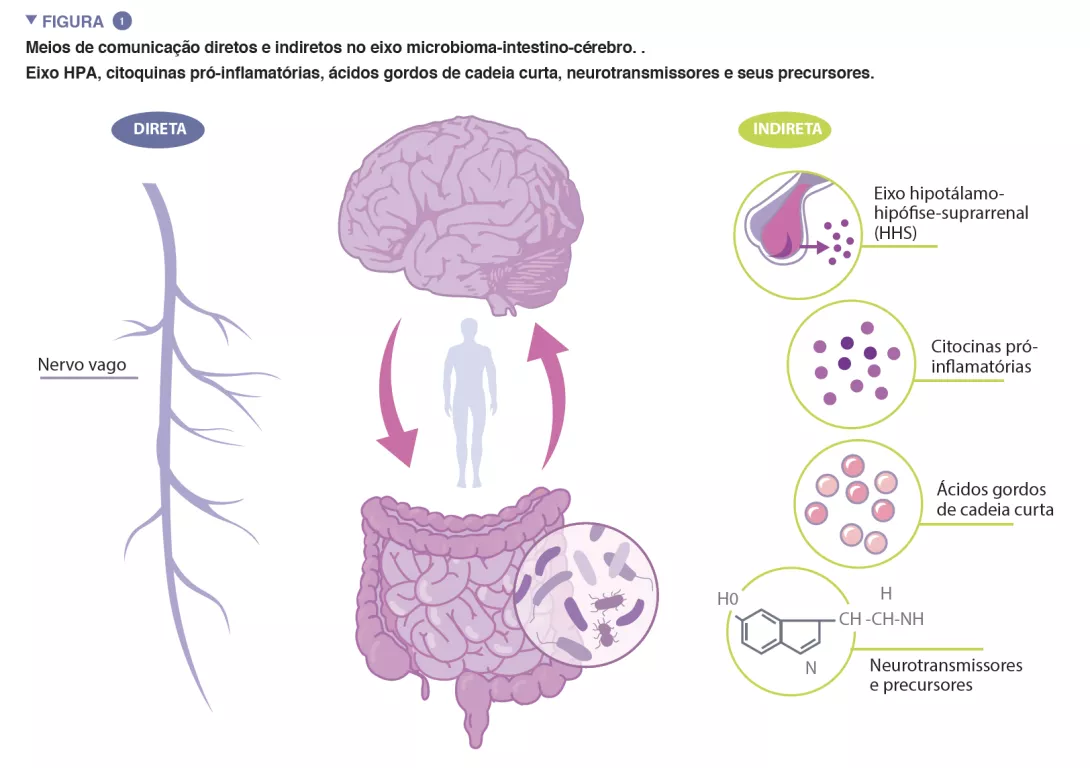
O nervo vago, o principal nervo parassimpático do sistema nervoso autónomo, representa uma ligação direta entre o intestino e o cérebro, com aferentes e eferentes vagais facilitando a interação recíproca entre o sistema nervoso entérico e o cérebro. A comunicação indireta dentro do eixo MGB assume muitas formas. A microbiota produz várias moléculas derivadas de micróbios, incluindo neurotransmissores e metabolitos, que atuam em múltiplos locais do corpo. Muitas destas moléculas, incluindo a serotonina (5-HT), foram encontradas para regular o comportamento, função cerebral e saúde. Até 95% da 5-HT no corpo é produzida nas células enterocromafínicas que revestem o intestino, e os níveis de 5-HT no intestino são influenciados por metabolitos microbianos, incluindo o indole, ácidos biliares e ácidos gordos de cadeia curta (SCFA). A 5-HT produzida no intestino não pode ultrapassar a barreira hematoencefálica (BHE) e, portanto, não pode afetar os níveis de 5-HT no cérebro. No entanto, estudos com animais fornecem evidências que sugerem que os níveis do precursor de 5-HT, triptofano, modulado por certas bactérias intestinais, estão associados à regulação da neurotransmissão de 5-HT no cérebro [7].
Verificou-se que as alterações nos SCFA, um produto da fermentação bacteriana dos polissacáridos indigeríveis do hospedeiro, foram associadas à exposição ao stress crónico e ao comportamento depressivo em estudos com animais. Os SCFA estão envolvidos numa série de funções reguladoras, incluindo a modulação da atividade intestinal e integridade intestinal, e a activação de microglia (células imunes inatas no cérebro, que desempenham um papel importante na regulação da sobrevivência e respostas neuronais). Os SCFA são capazes de atravessar a BHE, e ao fazê-lo, podem afetar a função cerebral.
Está bem estabelecido que o microbioma intestinal desempenha um papel importante no desenvolvimento tanto do sistema imunitário periférico como do sistema imunitário central, e a acumulação de provas sugere que o aumento da inflamação está associado a perturbações relacionadas com o stress. Um desequilíbrio na composição microbiana intestinal pode comprometer a integridade do epitélio intestinal [8], aumentando a permeabilidade intestinal e facilitando a translocação de bactérias, ou componentes bacterianos, através da barreira epitelial para a circulação sistémica. Isto promove uma inflamação de baixo grau, que estimula uma maior expressão de citocinas pró-inflamatórias. As citocinas pró-inflamatórias podem estimular o eixo hipotálamo-hipófise suprarrenal (HPA) para segregar o cortisol, o que pode aumentar ainda mais a permeabilidade intestinal. De facto, foram relatadas evidências de disfunção do intestino e da barreira cerebral em perturbações relacionadas com o stress.
A administração sistémica de lipopolissacáridos (LPS), um componente importante da membrana externa das bactérias gram-negativas, resultou em ansiedade aguda e aumento de sintomas de tipo depressivo, bem como défices cognitivos, e verificou-se que o aumento dos níveis de citocinas próinflamatórias induzido pelo LPS alterou a atividade neuronal em áreas límbicas do cérebro. Verificou-se também que o LPS induziu um aumento da produção de citocinas no SNC, comprometendo a integridade da BHE, resultando num “cérebro com fugas”.
Várias investigações pré-clínicas apoiam a ideia de que a composição microbiana intestinal está associada a perturbações relacionadas com o stress. As investigações que utilizam animais sem germes (GF, microbiologicamente estéreis) têm desempenhado um papel crucial na nossa compreensão do eixo MGB. Na sua investigação seminal, Sudo e colegas [9] observaram uma resposta exagerada ao stress, evidenciada pelo aumento dos níveis de corticosterona, em ratos GF, em comparação com os controlos, na sequência de stress agudo de contenção. Esta resposta exagerada do eixo HPA ao stress foi normalizada na mono-colonização dos ratos GF com Bifidobacterium infantum. Estudos demonstraram também que é possível transferir fenótipos comportamentais de ansiedade entre duas estirpes de ratos, por meio de transplante de microbiota fecal (FMT) [10]. Do mesmo modo, vários estudos relataram o desenvolvimento de comportamentos depressivos e ansiosos, e de vias neuroendócrinas alteradas, em roedores com microbiota, após FMT de humanos diagnosticados com MDD, sugerindo um papel causal para a microbiota intestinal em comportamentos depressivos [11-13]. Estudos com animais também demonstraram que a exposição ao stress pode causar alterações duradouras no microbioma intestinal - dois estudos recentes relataram a diminuição da abundância relativa de Akkermansia muciniphila no microbioma intestinal de animais stressados ao longo do tempo, em comparação com animais de controlo [14, 15]. A. muciniphila e a camada externa da membrana da bactéria (Amuc_1100) foram considerados como melhorando o comportamento depressivo, e aumentando os níveis circulatórios de 5-HT.
Comparativamente, poucos estudos clínicos foram realizados para determinar a associação entre o microbioma intestinal e as perturbações relacionadas com o stress. Até agora, os únicos dados publicados sobre o microbioma intestinal no PSPT emanam do nosso grupo de investigação [16], onde foi encontrado um consórcio de quatro géneros bacterianos para prever o estado do PSPT com 66,4% de exatidão. Além disso, verificou-se que o diagnóstico MDD na amostra estava associado ao aumento da abundância relativa do filo Bacteroidetes. Outros estudos indicam que os taxa bacterianos associados tanto à depressão como às perturbações de ansiedade se caracterizam por uma maior abundância relativa de taxa que induzem um ambiente pró-inflamatório e uma reduzida abundância de bactérias produtoras de SCFA [17].
O campo da investigação está, no entanto, ainda na sua infância, atualmente limitado pela falta de normalização na análise microbiológica intestinal, desde a recolha de amostras aos métodos analíticos. Em muitos casos, fatores que podem confundir os resultados, incluindo dieta, uso de medicamentos, etnia e genética do hospedeiro, não foram tidos em conta nos estudos analisados acima. Além disso, a maioria dos estudos realizados foram transversais na conceção, limitando a nossa capacidade de separar as causas das consequências, e muito poucos investigaram mecanismos potenciais subjacentes às associações.
A. muciniphila é uma bactéria anaeróbica gram-negativa, encontrada principalmente na mucosa intestinal, e desempenha um papel na manutenção da integridade da barreira intestinal, bem como na regulação imunológica e metabólica.
O microbioma intestinal é rastreável e tem o potencial de ser modulado, tornando a procura de marcadores microbiológicos intestinais associados a perturbações relacionadas com o stress particularmente atrativa. Os probióticos são definidos como microrganismos vivos que, quando administrados em quantidades adequadas, conferem um benefício para a saúde do hospedeiro; os psicobióticos referem-se aos probióticos que conferem um benefício para a saúde mental, cognição e comportamento. Publicações recentes indicaram efeitos benéficos moderados dos psicobióticos no alívio de sintomas depressivos e de ansiedade, tanto em coortes saudáveis como em coortes clinicamente definidas [18]. No entanto, é importante manter-se cauteloso na interpretação dos resultados dos estudos atuais, uma vez que são variáveis no que diz respeito à formulação e dosagem probiótica, características da amostra (fenótipo clínico e gravidade da depressão/ansiedade), e tempo de seguimento. Além disso, o benefício dos psicobióticos sobre, e as interações com, os medicamentos antidepressivos ainda não foi extensivamente investigado, embora alguns resultados intrigantes de estudos pré-clínicos sugiram que certos probióticos, quando administrados em formato multi-estirpe, possuem efeitos antidepressivos semelhantes aos, e por vezes com maior efeito do que os atuais antidepressivos de primeira linha [19]. Tais psicóticos, quando usados em conjunto com antidepressivos, podem ter uma utilização particular em indivíduos com depressão resistente ao tratamento.
As provas que sugerem que o microbioma intestinal é alterado em doenças relacionadas com o stress continuam a crescer, e embora ainda haja muito trabalho a fazer no terreno, delinear um perfil microbiano intestinal específico associado ao desenvolvimento de doenças relacionadas com o stress pode facilitar a identificação de biomarcadores fiáveis de risco associado à doença e prever a predisposição para desenvolver essas doenças. O microbioma intestinal pode ser facilmente manipulado e pode, portanto, oferecer uma opção de tratamento simples e sustentável para aliviar os sintomas de PSPT, MDD e distúrbios de ansiedade.
• 1. GBD 2019 Mental Disorders Collaborators. Global, regional, and national burden of 12 mental disorders in 204 countries and territories, 1990–2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet Psychiatry 2022; 9: 137-50.
• 2. van Praag HM. Can stress cause depression? Prog Neuropsychopharmacol Biol Psychiatry 2004; 28: 891-907.
• 3. Shin LM, Liberzon I. The neurocircuitry of fear, stress, and anxiety disorders. Neuropsychopharmacol 2010; 35: 169-91.
• 4. De Filippo C, Cavalieri D, Di Paola M, Ramazzotti M, Poullet JB, Massart S, et al. Impact of diet in shaping gut microbiota revealed by a comparative study in children from Europe and rural Africa. Proc Natl Acad Sci USA 2010; 107: 14691-6.
• 5. Schnorr SL, Candela M, Rampelli S, Centanni M, Consolandi C, Basaglia G. Gut microbiome of the Hadza hunter-gatherers. Nat Commun 2014; 5: 3564.
• 6. Ayeni FA, Biagi E, Rampelli S, et al. Infant and Adult Gut Microbiome and Metabolome in Rural Bassa and Urban Settlers from Nigeria. Cell Rep 2018; 23: 3056-67.
• 7. Clarke G, Grenham S, Scully P, et al. The microbiome-gut-brain axis during early life regulates the hippocampal serotonergic system in a sex-dependent manner. Molecular Psychiatry 2013; 18: 666-73.
• 8. Desbonnet L, Garrett L, Clarke G, Kiely B, Cryan JF, Dinan TG. Effects of the probiotic Bifidobacterium infantis in the maternal separation model of depression. Neuroscience 2010; 170: 1179-88.
• 9. Sudo N, Chida Y, Aiba Y, Sonoda J, Oyama N, Yu XN. Postnatal microbial colonization programs the hypothalamic-pituitary-adrenal system for stress response in mice. J Physiol 2004; 558: 263-75.
• 10. Bercik P, Denou E, Collins J, et al. The intestinal microbiota affect central levels of brain-derived neurotropic factor and behavior in mice. Gastroenterology 2011; 141: 599-609.
• 11. Kelly JR, Borre Y, O’ Brien C, Patterson E, El Aidy S, Deane J, et al. Transferring the blues: Depression-associated gut microbiota induces neurobehavioural changes in the rat. J Psychiatr Res 2016; 82: 109-18.
• 12. Liu S, Guo R, Liu F, Yuan Q, Yu Y, Ren F. Gut microbiota regulates depression-like behavior in rats through the neuroendocrine-immune-mitochondrial pathway. Neuropsychiatr Dis Treat 2020; 16: 859-69.
• 13. Zheng P, Zeng B, Zhou C, et al. Gut microbiome remodeling induces depressive-like behaviors through a pathway mediated by the host’s metabolism. Mol Psychiatry 2016; 21: 786-96.
• 14. Hoke A, Chakraborty N, Gautam A, Hammamieh R, Jett M. Acute and delayed effects of stress eliciting post-traumatic stress-like disorder differentially alters fecal microbiota composition in a male mouse model. Front Cell Infect Microbiol 2022; 12: 810815.
• 15. Pascual Cuadrado D, Todorov H, Lerner R, et al. Long-term molecular differences between resilient and susceptible mice after a single traumatic exposure. Br J Pharmacol 2022; 179: 4161-80.
• 16. Malan-Muller S, Valles-Colomer M, Foxx CL, et al. Exploring the relationship between the gut microbiome and mental health outcomes in a posttraumatic stress disorder cohort relative to trauma-exposed controls. Eur Neuropsychopharmacol 2022; 56: 24-38.
• 17. Simpson CA, Diaz-Arteche C, Eliby D, Schwartz OS, Simmons JG, Cowan CSM. The gut microbiota in anxiety and depression - A systematic review. Clin Psychol Rev 2021;83: 101943.
• 18. Alli SR, Gorbovskaya I, Liu JCW, Kolla NJ, Brown L, Müller DJ. The gut microbiome in depression and potential benefit of prebiotics, probiotics and synbiotics: a systematic review of clinical trials and observational studies. Int J Mol Sciences 2022; 23: 4494.
• 19. Ra Y, Eu P, Ev V, Mv O, Mv M, Gi K, et al. A Multi-strain potential probiotic formulation of GABA-producing Lactobacillus plantarum 90sk and Bifidobacterium adolescentis 150 with antidepressant effects. Probiotics and Antimicrobial Proteins 2020; 12: 973-9.
O consumo de refeições “pronto a comer”, por mais equilibradas que elas sejam, não será isento de consequências para a nossa saúde. Efetivamente, as bandejas em que esses alimentos são servidos contêm microplásticos que afetam nossa microbiota.

As bandejas plásticas das refeições “pronto a comer” ou “takeaway” libertam microplásticos e nanoplásticos que terão repercussões significativas na microbiota oral e intestinal dos consumidores.
Em 2020, um estudo mostrou que embalagens plásticas para alimentos (polipropileno PP, poliestireno PS, polietileno PE e polietileno tereftalato PET) continham micro e nanoplásticos. Embora os efeitos nocivos destas partículas sobre a microbiota já tenham sido demonstrados em animais (peixes, camarões e ratos), têm sido até agora pouco estudados nos seres humanos.
Os investigadores analisaram e compararam a microbiota intestinal e oral de um grupo de 390 estudantes chineses com idades compreendidas entre os 18 e os 30 anos, que consumiam comida “takeaway” servida em bandejas de plástico com frequência (pelo menos 3 vezes por semana), ocasionalmente (uma vez por semana ou menos) ou nunca.
Em paralelo, os cientistas criaram 4 grupos de ratos aos quais deram ou uma solução de microplásticos a 5 mg/ml (20 ratos), ou uma solução de nanoplásticos a 5 mg/ml (20 ratos), ou uma solução dos mesmos nanoplásticos, mas a 2 mg/ml (20 ratos) e, finalmente, um grupo de controlo de 15 ratos.
Os resultados mostram que os consumidores de alimentos “pronto a comer” sofrem de mais perturbações intestinais e tossem mais do que aqueles que nunca os consomem. Surge igualmente uma disbiose nas microbiotas intestinal e oral com assinaturas bacterianas específicas. Enquanto a microbiota intestinal dos utilizadores ocasionais se manifestou fortemente associada à presença de Faecalibacterium, na dos grandes consumidores a predominância pertencia à bactéria Collinsella. A nível oral, a bactéria Thiobacillus foi a que surgiu mais fortemente associada à microbiota dos grandes consumidores.
O estudo sobre ratos mostra que todos os animais alimentados com partículas de plástico apresentaram disbiose intestinal em comparação com o grupo de controlo. A ingestão de partículas de tamanhos diferentes (micro vs. nanopartículas) e de quantidade reduzida (5 mg/ml vs. 2 mg/ml) resulta no mesmo efeito.
Além disso, a recorrência de uma tosse nos consumidores de alimentos de takeaway poderá significar, segundo os cientistas, que os micro e nanoplásticos são capazes de migrar do intestino para os pulmões, acumular-se na microbiota das vias respiratórias e levar à disbiose que causa a tosse. Até que estes resultados sejam confirmados, trata-se de um argumento adicional para preferir os recipientes de vidro durante o almoço.
 Doenças Inflamatórias Crónicas do Intestino (DICI): os microplásticos estão envolvidos na sua gravidade?
Doenças Inflamatórias Crónicas do Intestino (DICI): os microplásticos estão envolvidos na sua gravidade?
 Tudo o que necessita de saber sobre disbiose
Tudo o que necessita de saber sobre disbiose
Embora vacinadas, algumas crianças não desenvolvem imunidade protetora, particularmente em países de baixos e médios rendimentos. A microbiota intestinal, intimamente ligada ao funcionamento imunitário, pode ser um dos fatores por trás dessa variabilidade nas respostas vacinais.
Reconhecidamente, a vacinação é um dos maiores sucessos de saúde pública, salvando milhões de vidas em todo o mundo, principalmente entre as crianças mais pequenas (0-5 anos), que são mais vulneráveis às doenças infeciosas. No entanto, a sua eficácia varia de uma população para outra, com níveis mais altos de imunidade protetora nos países europeus em comparação com os países de baixos e médios rendimentos (PBMR). Embora o desenvolvimento da microbiota intestinal no início da vida esteja intimamente ligado à maturação do sistema imunitário e a microbiota das crianças nos PBMR difira significativamente da das crianças europeias, os investigadores compilaram numa revisão as provas que apontam para o papel da microbiota intestinal nas disparidades nas respostas vacinais.
Nela descobrimos que a presença de certos táxons está correlacionada com a taxa de resposta à vacina: positiva para Actinobacteria, mas negativa para Enterobacteriaceae, num estudo sobre as vacinas contra a tuberculose, o tétano, a hepatite B e a poliomielite nos lactentes do Bangladesh. Para além destas observações, as intervenções destinadas a modificar a microbiota (prebióticos, probióticos, antibióticos) testemunham também o seu envolvimento na resposta vacinal. Uma revisão sistemática de 2018 resumiu os resultados de 26 ensaios realizados com probióticos em seres humanos para melhorar a eficácia de diferentes vacinas. Ela constata a existência de efeitos positivos em metade dos casos. Simetricamente, os estudos que testaram os efeitos dos antibióticos detetaram ausência de efeitos ou uma redução na resposta imunitária, atribuída à perturbação da microbiota.
Dois géneros bacterianos parecem ser particularmente capazes de modular as respostas à vacinação: Bifidobacterium e Bacteroides, comunidades que são essenciais para o desenvolvimento de uma microbiota saudável nos bebés, mas que poderão provavelmente sofrer perturbações significativas nessa etapa da vida (cesariana, entre outras). Os efeitos da microbiota nas respostas vacinais serão mediados por certos metabolitos e/ou componentes celulares, como os ácidos gordos de cadeia curta, os exopolissacarídeos ou as vesículas extracelulares.
Embora as cepas e os produtos de interesse mereçam ser melhor caraterizados, as perspetivas clínicas abertas pela intrincada relação entre a microbiota e a eficácia vacinal são ricas. Objetivo: novas terapias de estimulação vacinal, potencialmente desprovidas de adjuvantes (muitas vezes suspeitos de efeitos adversos) e capazes de melhorar a proteção das crianças dos PBMRs.
Como sabemos, a microbiota intestinal difere de um indivíduo para outro. Essa diferença poderá explicar variações na eficácia da vacina, com respostas mais pobres entre as crianças nos países de baixos rendimentos. Estão em estudo estratégias que visam modificar a composição da microbiota intestinal para reparar essa “injustiça imunitária”.
A microbiota intestinal
Em teoria, o princípio da vacinação é simples (ou quase): (sidenote: Isso é feito através da inoculação do organismo com um fragmento inofensivo do inimigo para que ele desenvolva defesas específicas. No caso de um encontro subsequente com o verdadeiro agente patogénico, as defesas estão prontas para neutralizar o invasor. https://www.who.int/fr/emergencies/diseases/novel-coronavirus-2019/covid-19-vaccines/how-do-vaccines-work ) Só que, na prática, isto não funciona para todos: embora salve milhões de vidas todos os anos, especialmente de crianças pequenas que são mais suscetíveis a doenças infeciosas, a vacinação é mais eficaz para as crianças europeias do que para as de países de baixos e médios rendimentos (PBMR). Embora vacinadas, (sidenote: Enquanto quase 100% das crianças finlandesas desenvolvem imunidade protetora em resposta à vacinação contra o rotavírus, apenas 58% das crianças na Nicarágua e 46% no Bangladesh o conseguem. Da mesma forma, as taxas de proteção em resposta à vacina BCG variam entre 0 e 51% em África contra 88% a 100% nas crianças europeias. ) Por outras palavras, o seu exército de anticorpos ( (sidenote: Imunidade inata e adaptativa O corpo humano garante a sua proteção graças a 2 tipos de mecanismos de defesa: a imunidade inata e a imunidade adaptativa. A imunidade inata é a primeira linha de defesa contra os agentes infeciosos, sendo uma reação imediata. Por sua vez, a imunidade adaptativa intervém mais tarde, mas visa uma proteção duradoura Janeway CA Jr, Travers P, Walport M, et al. Immunobiology: The Immune System in Health and Disease. 5th edition. New York: Garland Science; 2001. Principles of innate and adaptive immunity. ) ) não consegue reagir. Não estando treinado para reconhecer e erradicar o inimigo, ele tem poucas chances de conseguir defender a sua posição quando ocorre um combate verdadeiro... Mas como explicar tamanha “injustiça imunitária”?
A resposta poderá estar nos batalhões de uma terceira força especial, aliada ao exército imunitário: a microbiota intestinal. De facto, não só o desenvolvimento e funcionamento da microbiota intestinal e do sistema imunitário estão intimamente ligados, mas a microbiota intestinal das crianças europeias é também muito diferente da das crianças dos PBMR. Para os investigadores, as diferenças na composição da microbiota poderão, assim, explicar a variação nas respostas vacinais. Neste contexto, há estudos que têm procurado modificar a microbiota intestinal para melhorar a resposta imunitária. Em metade dos ensaios em seres humanos, a administração de probióticos bactérias vivas que aumentam as fileiras da microbiota) aumenta a proporção de pacientes que desenvolvem imunidade protetora. Duas sentinelas da microbiota intestinal, os gêneros bacterianos
(sidenote:
Bifidobactérias
Bactérias em forma de bastonete, em Y. A maioria das espécies são benéficas para os seres humanos. Encontram-se no intestino humano, e também em alguns iogurtes.
Estas bactérias:
- Protegem a barreira intestinal
- Participam no desenvolvimento do sistema imunológico e ajudam a lutar contra a inflamação
- Promovem a digestão e aliviam os sintomas gastrointestinais
Sung V, D'Amico F, Cabana MD, et al. Lactobacillus reuteri to Treat Infant Colic: A Meta-analysis. Pediatrics. 2018 Jan;141(1):e20171811.
O'Callaghan A, van Sinderen D. Bifidobacteria and Their Role as Members of the Human Gut Microbiota. Front Microbiol. 2016 Jun 15;7:925.
Ruiz L, Delgado S, Ruas-Madiedo P, et al. Bifidobacteria and Their Molecular Communication with the Immune System. Front Microbiol. 2017 Dec 4;8:2345.
)
e Bacteroides, parecem particularmente capazes de estimular as tropas imunitárias.
Embora seja ainda necessária mais investigação, os investigadores já estão a ponderar novas estratégias de vacinação que poderão envolver a modulação da composição da flora intestinal para estimular a resposta às vacinas. Trata-se de uma nova abordagem que deverá aumentar as possibilidades de acesso a uma imunização eficaz nos países de baixo e médio rendimento (PBMR). Esta abordagem permitiria também eliminar certos adjuvantes, que são adicionados para aumentar a resposta imunitária mas que são suspeitos de ter efeitos indesejáveis, suscitando a desconfiança em relação às vacinas.
Jordan A, Carding SR, Hall LJ. The early-life gut microbiome and vaccine efficacy. Lancet Microbe. 2022 Oct;3(10):e787-e794. doi: 10.1016/S2666-5247(22)00185-9.
 Cancro do pulmão: uma (super)bactéria para se prever melhor a eficácia dos tratamentos
Cancro do pulmão: uma (super)bactéria para se prever melhor a eficácia dos tratamentos
