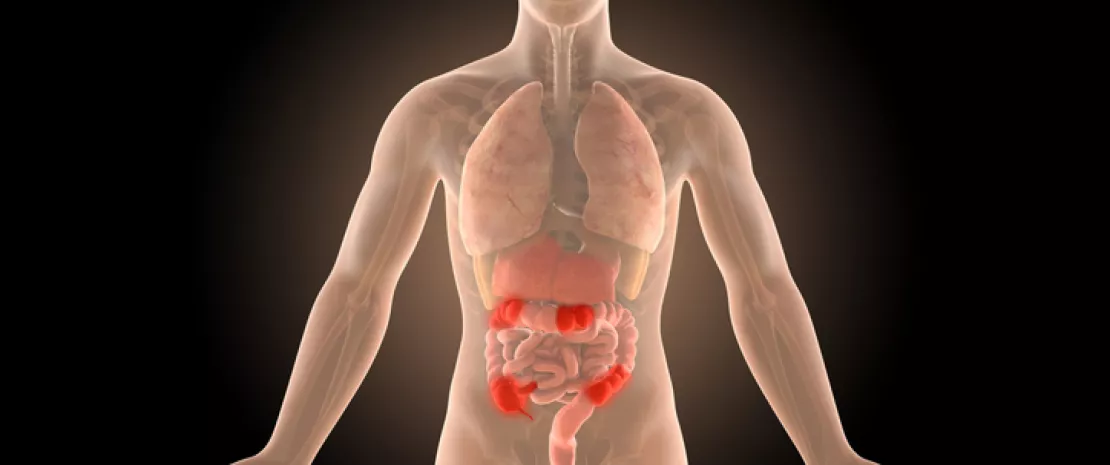
Волчанка, также называемая системной красной волчанкой, является аутоиммунным заболеванием. Микробиота кишечника возможно играет роль в развитии этого заболевания.
Трудно определить количество людей, страдающих волчанкой. По разным оценкам распространенность этого заболевания во всем мире варьируется от 10 до 150 случаев на каждые 100 000 жителей, большинство из которых составляют женщины (85 %).
Когда иммунная система атакует собственные клетки
По причинам, которые остаются неизвестными, иммунная система у людей, страдающих волчанкой, производит аутоантитела, которые вызывают воспалительные реакции и поражения всех тканей. Волчанка имеет целый ряд симптомов: усталость, кожные высыпания, боль в суставах, сухость глаза, выпадение волос, тромбоз, жар, плеврит и перикардит. Это заболевание прогрессирует во время обострений разной продолжительности и интенсивности, которые чередуются с периодами ремиссии. Диагноз волчанки подтверждается анализом крови, и степень повреждения измеряется с помощью методов медицинской визуализации.
Предрасполагающие факторы, но неизвестная причина
Хотя причины волчанки остаются загадкой, было определено несколько предрасполагающих факторов: эстроген, генетическая предрасположенность, определенные лекарственные препараты, УФ-лучи, стресс и некоторые вирусы (вирус Эпштейна – Барр). В ходе исследований также была изучена роль кишечной микробиоты. Бесспорно, дисбаланс (дисбиоз) наблюдался у пациентов с волчанкой во время периода ремиссии. Микробиота может даже участвовать в производстве аутоантител.
Сократить число и длительность приступов
Волчанка является неизлечимым заболеванием. Однако сочетание нескольких препаратов (нестероидные противовоспалительные средства, противомалярийные средства, кортикостероиды, иммунодепрессанты и моноклональные антитела в зависимости от тяжести заболевания) облегчает обострения, ограничивает осложнения и удлиняет периоды ремиссии. В то же время менее суровые долгосрочные методы лечения предотвращают рецидивы.
Если подтвердится роль микробиоты, то ее модулирование с помощью диеты или пробиотиков может стать перспективным вариантом терапии.