Que sait-on déjà à ce sujet ?
Le nombre d'enfants ayant une allergie alimentaire est en forte augmentation, représentant actuellement 28% des enfants américains âgés de 1 à 5 ans. La mise en place du microbiote intestinal (MI) au cours des premiers mois de vie pourrait être impliquée dans cette sensibilisation aux allergènes alimentaires [2]. De nombreux facteurs influencent l'établissement du MI, comme le mode d'accouchement (césarienne vs voie vaginale), le type d’allaitement (maternel ou formules infantiles) et l’utilisation d’antibiotiques [3, 4]. Une étude récente a montré que la structure du MI variait aussi significativement entre différents groupes ethniques [5].
Par ailleurs, le transfert de MI d’enfants sains à des souris protège celles-ci de l’allergie aux protéines du lait de vache. Un MI pauvre chez le jeune nourrisson et un taux élevé d’Enterobacteriaceae/Bacteroidaceae (E/B) chez les nourrissons jeunes et âgés sont des facteurs prédicitifs de sensiblisation aux allergènes alimentaires [6].
Quels sont les principaux résultats apportés par cette étude ?
L’étude a inclus 1 422 enfants de la cohorte CHILD (Canadian Healthy Infant Longitudinal Development), et des des prick-tests ont été réalisés (pneumallergènes et allergènes alimentaires) à l’âge de 1 et 3 ans. Des échantillons de selles ont été prélevés précocement (3,5 ± 0,9 mois) et tardivement (12,2 ± 0,3 mois).
La prévalence d’atopie était de 12 % à 1 an et de 12,8 % à 3 ans, avec 9,5 et 5,8 % de sensibilisation alimentaire et 3,3 et 10,1 % de sensibilisation aux pneumallergènes à 1 et 3 ans respectivement.
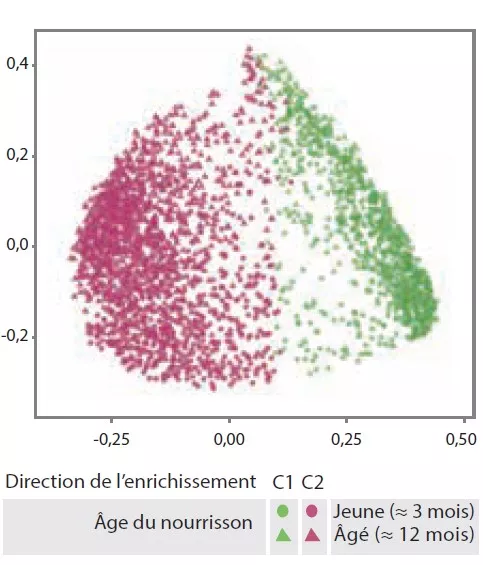
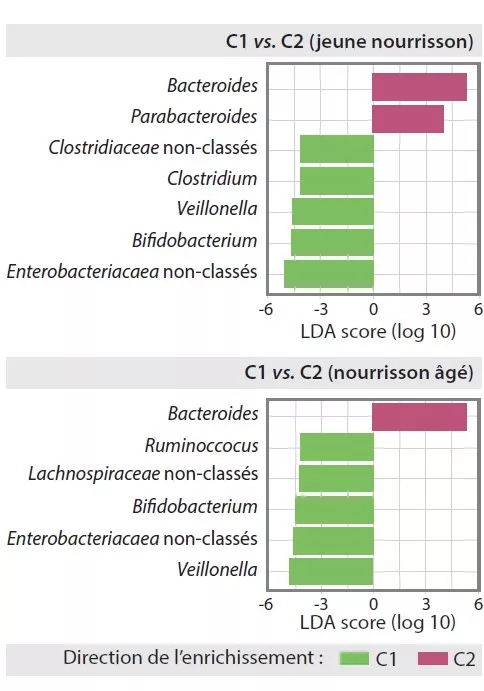
Le MI tardif avait une diversité béta et une variabilité intra-individuelle plus faibles que le MI précoce (p < 0,001). Le MI tardif était enrichi en Bacteroides, Faecalibacterium, Lachnospira, Prevotella, Lachnospiraceae non-classés et Clostridiales non classés, mais pauvre en Clostridium, Veillonella, Bifidobacterium et Enterobacteriaceae non classés. L’analyse en composantes principales avait permis d’individualiser 2 clusters (C1 et C2, Figure 1). C1 était composé à 75,5 % d’échantillons précoces et C2 à 63,7 % d’échantillons tardifs ; les échantillons précoces et tardifs des enfants nés par voie basse sans antibioprophylaxie intrapartum étaient de type C2, dominés par le genre Bacteroides (Figure 2).
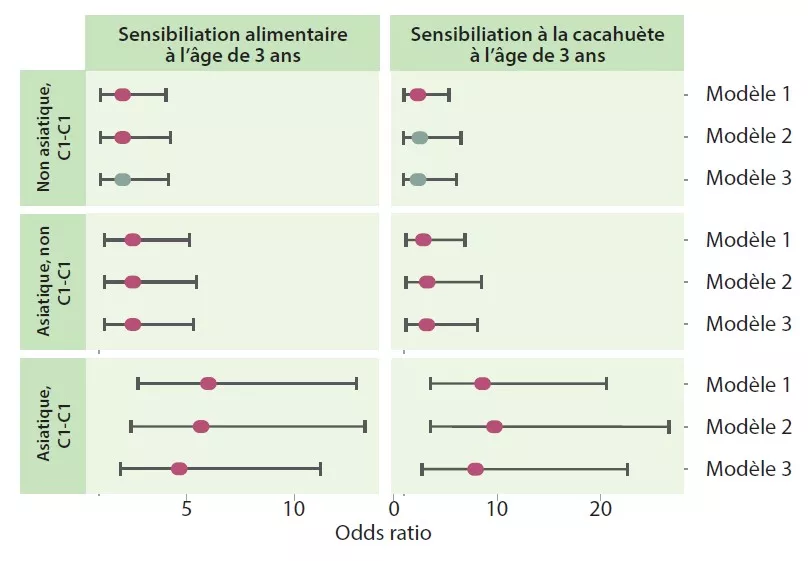
Les auteurs ont déterminé 4 trajectoires en fonction du type de cluster précoce et tardif : C1-C1, C1-C2, C2-C1 et C2-C2. La trajectoire C1-C1 est plus fréquente chez les nourrissons asiatiques que caucasiens (p < 0,05), de même que chez les enfants à risque atopique vs la trajectoire C2-C2 (OR 1,9 ; IC 95 % 1,15-3,14) ou C1-C2 (OR 2,38 ; IC 95 % 1,43-3,96). Les nourrissons de la trajectoire C1-C1 avaient 2 fois plus de risques de sensibilisation alimentaire à 3 ans que ceux des trajectoires C2-C2 (OR 2,34 ; IC 95 % 1,20-4,56) et C1-C2 (OR 2,60 ; IC 95 % 1,33-5,09), notamment à la cacahuète (vs C2-C2 = OR 2,82 ; IC 95% 1,13-6,01 et vs C1-C2 = OR 2,01 ; IC 95% 0,85-4,78) (Figure 3). Les enfants qui n’acquéraient pas de sensibilisation à la cacahuète à 3 ans avaient, de manière persistante, au cours de l’enfance, un taux plus élevé de Bacteroides (p = 0,044), plus bas d’Enterobacteriaceae non classés (p = 0,001) et un ratio E/B plus bas (p = 0,013).
La trajectoire C1-C1 du MI jouait le rôle de médiateur du risque de sensibilisation alimentaire et à la cacahuète chez les enfants d’origine asiatiques. L’association était même forte pour la cacahuète (OR 7,87 ; IC 95 % 2,75-22,55). Les nourrissons de la trajectoire C1-C1 étaient plus souvent colonisés avec C. difficile ; ces mêmes enfants, à la double caractéristique C1-C1 et colonisés à C. difficile, avaient un risque supérieur de sensibilisation alimentaire (OR 5,69 ; IC 95 % 1,62-19,99) et à la cacahuète (OR 5,89 ; IC 95% 1,16-29,87).
Enfin, le microbiote de la trajectoire C1-C1 avait un déficit dans le métabolisme des sphingolipides et de fonctions liées à la biosynthèse des glycosphingolipides.
Quelles sont les conséquences en pratique ?
Cette étude permet d’envisager des perspectives thérapeutiques ciblant le MI dans l’allergie alimentaire des nourrissons, soit en préventif, soit en thérapeutique.