Hе переоцениваем ли мы значение микро- биоты урогенитальной области?
В последние годы наше представление об урогенитальной микробиоте стало более определенным. Нам уже известно, что она может играть определенную роль в развитии инфекций, заболеваний мочевыводящих путей, связанных с менопаузой, и даже опухолей. Фактор урогенитальной микробиоты и ее нарушения следует учитывать при ведении пациентов, а пробиотики должны стать частью терапевтического арсенала. Разумеется, пробиотики — это не единственное наше оружие, однако следует признать их ключевую роль, поскольку противоинфекционные методы лечения не воздействуют на причину рецидива, которой является дисбиоз.
Как вы думаете, какую роль сегодня могут играть пробиотики при лечении инфекций мочевыводящих путей?
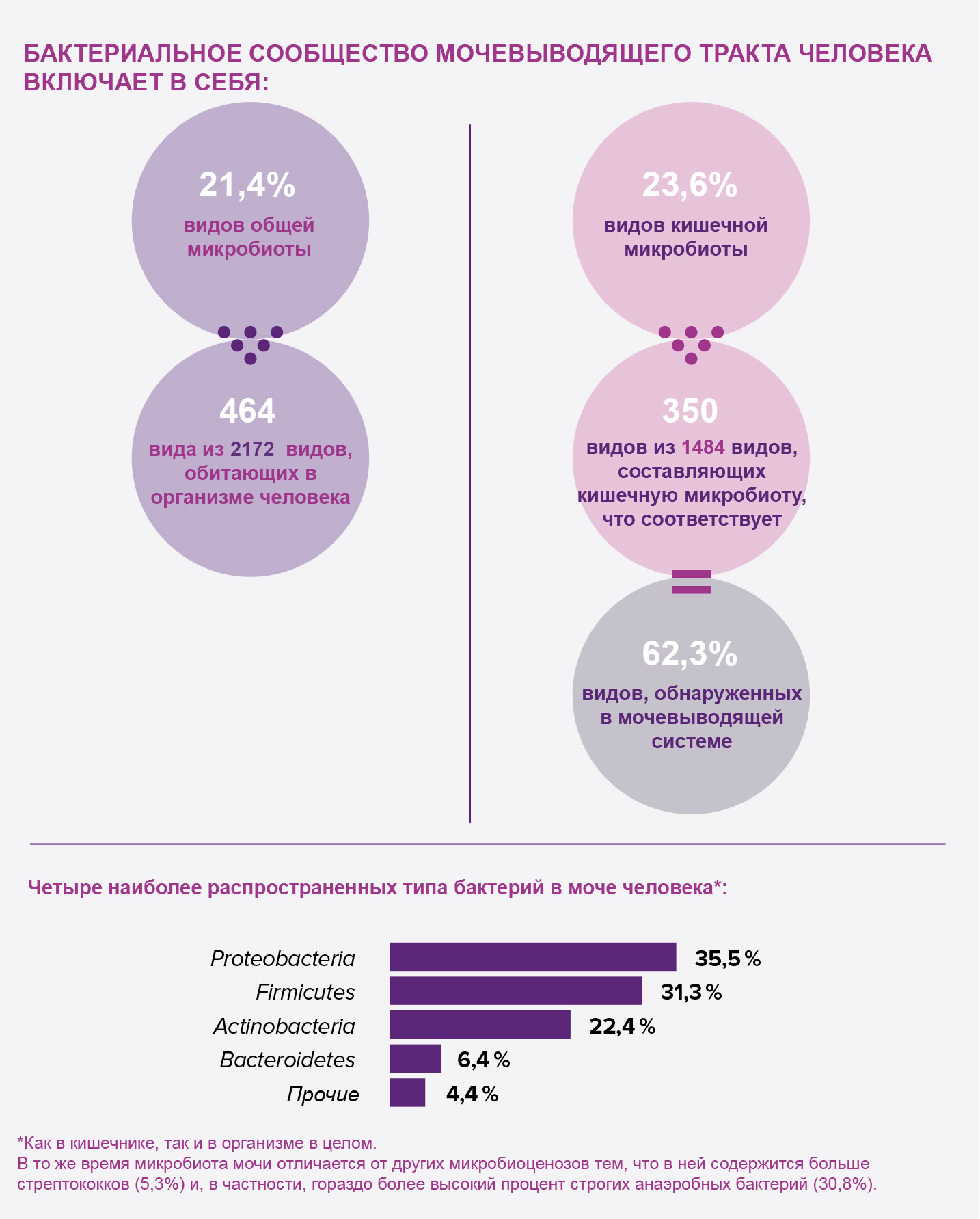
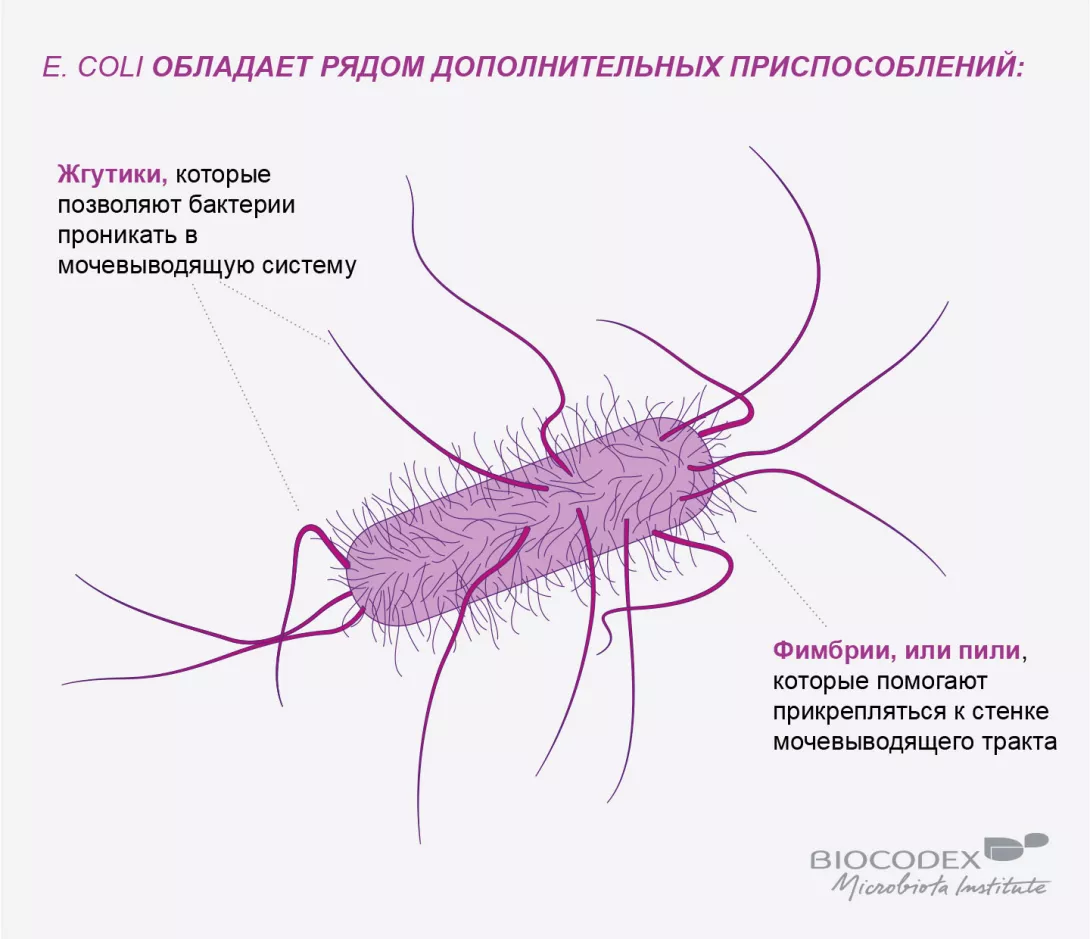
Инфекции мочевыводящих путей тесно связаны с дисбалансом в трех микробиомах: в микробиоте мочи, поскольку моча не является стерильной, в вагинальной микробиоте, с которой микробиота мочи имеет много общего, и в микробиоте кишечника, из которой проникают патогенные микроорганизмы, являющиеся возбудителями инфекций мочевыводящих путей (например, E. coli, которая перемещается из анальной области до преддверия влагалища и затем в мочевой пузырь).
Традиционную антибактериальную терапию целесообразно использовать при лечении единичных эпизодов ИМП. В тех случаях, когда речь идет о рецидивах ИМП (более четырех эпизодов в год), после исключения органических причин (например, опухоли мочевого пузыря) важно выяснить, есть ли у пациентки возможные признаки нарушения кишечной микробиоты (запор и т. д.) и/или микробиоты влагалища. Следует помнить, что вагинальная микробиота действует как защитный барьер между пищеварительной и мочевыводящей системами. Профилактика рецидива включает применение пероральных кишечных пробиотиков на протяжении от трех до шести месяцев в тех случаях, когда есть сопутствующий дисбиоз кишечной микробиоты, и/или вагинальных пробиотиков, в идеале предназначенных для интравагинального введения. Эти методы лечения можно сочетать с употреблением клюквы, которая способствует снижению содержания E. coli в мочевом пузыре.
Что важно знать о вагинальных инфекциях?
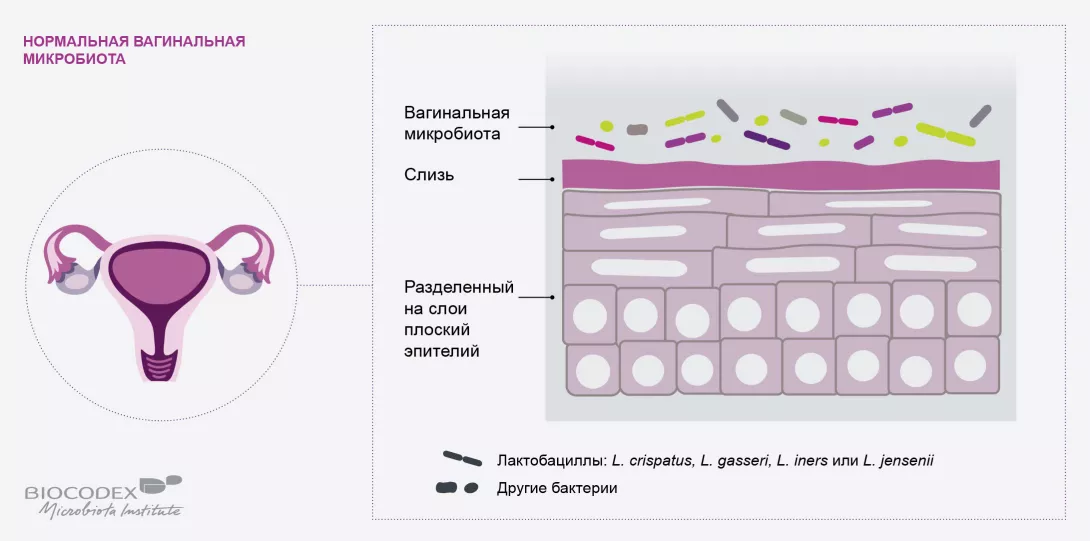
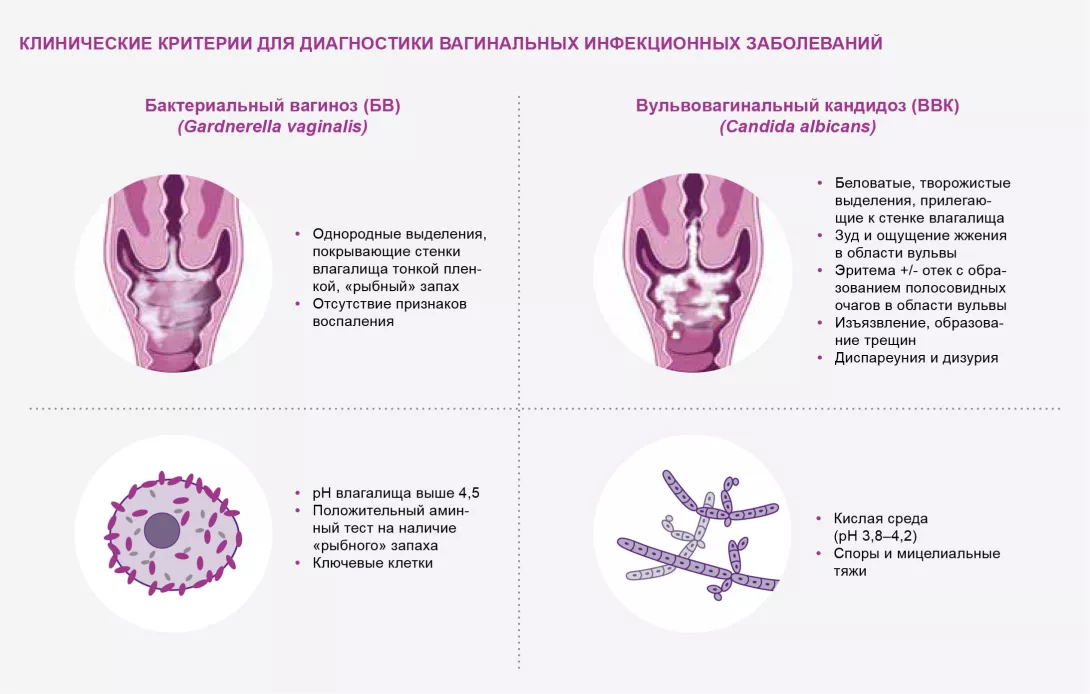
Существует два типа вагинальных инфекций: эндогенные, возникающие в результате изменений в видовом составе микроорганизмов (бактерий или грибов), населяющих организм, и экзогенные, заражение которыми происходит при половых контактах. Когда речь идет об эндогенных инфекциях, в случае единичного эпизода будет достаточно применения вагинальных суппозиториев с противогрибковым средством или антибиотиков. Однако при наличии риска рецидива необходимо лечение дисбиоза в течение нескольких месяцев с использованием гинекологических пробиотиков. Пробиотики также играют роль в лечении экзогенных инфекций, поскольку чем менее сбалансирована вагинальная микробиота, тем выше риск заражения инфекциями, передаваемыми половым путем (ИППП), и выше риск неблагоприятного исхода. Например, при наличии дисбиоза частота неуспешной полной эрадикации вируса папилломы человека в четыре-пять раз выше и наблюдается более быстрое прогрессирование злокачественной трансформации. Поэтому инфицированных женщин важно обследовать на наличие дисбаланса вагинальной микробиоты путем простого измерения кислотности среды (pH должен находиться в диапазоне от 3,5 до 4,5), а в тех случаях, когда pH превышает 4,5, — с последующим взятием и оценкой образцов выделений. При выявлении дисбаланса следует назначить пробиотики, прошедшие лабораторную оценку и одобренные для клинического применения. Дисбиоз влагалища также повышает риск заражения вирусом иммунодефицита человека (ВИЧ). Несмотря на то что кислая среда, создаваемая лактобациллами, помогает уничтожить вирус, воспалительное состояние приводит к повышению содержания лимфоцитов, которые являются мише- нью для ВИЧ..
Наконец, каковы перспективы трансплантации ва- гинальной микробиоты?
На сегодняшний день опубликованы результаты более чем двадцати случаев трансплантации вагинальной микробиоты. Безусловно, эти результаты вызывают интерес, но они не являются окончательными. Идея лечения рецидивирующего бактериального вагиноза посредством трансплантации микробиоты по-прежнему вызывает обеспокоенность с точки зрения критериев отбора доноров, особенно в связи с тем, что отсутствие симптомов не означает сбалансированности микробиоты донора. Кроме того, неясны показания для реципиента. Вероятнее всего, через год-два станет известно, можно ли использовать трансплантаты вагинальной микробиоты в качестве средства последнего выхода.