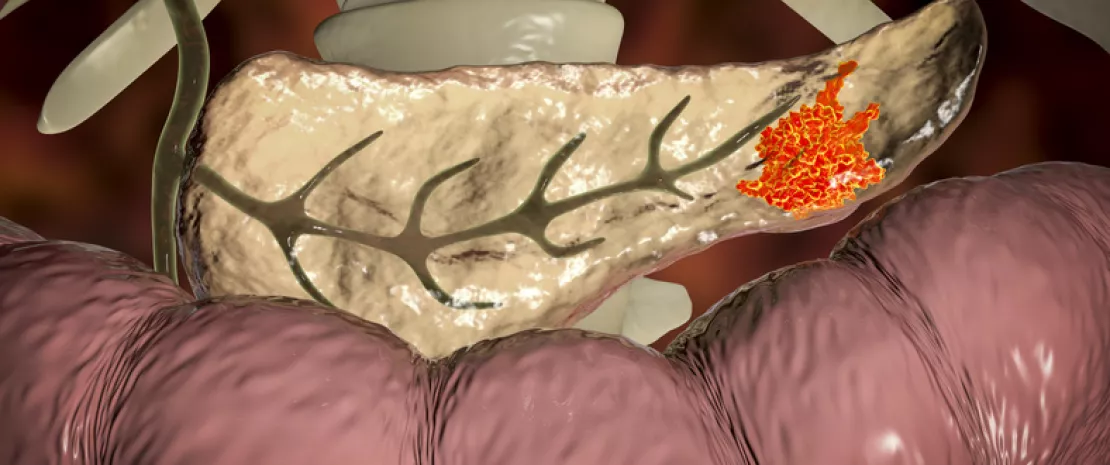
Протоковая аденокарцинома поджелудочной железы (PDAC) – страшное онкологическое заболевание. Так как она обычно диагностируется поздно, при общей выживаемости в 9 % в течение 5 лет прогноз неутешителен. По-видимому, микробиота опухоли имеет значение для данной выживаемости, что подтверждают многочисленные результаты, опубликованные в журнале Cell группой исследователей из Америки.
Больше разнообразие – больший процент выживаемости
Чтобы изучить влияние микробиоты опухоли и иммунной системы на выживаемость, эти исследователи проанализировали состав микробиоты резецированных опухолей у 68 пациентов с PDAC, распределенных на две группы: 36 пациентов с более чем 5-летней выживаемостью (среднее значение: 10,1 года), и 32 пациента, умерших в течение 5 лет после операции (среднее значение: 1,6 года). Результаты, полученные этими исследователями, свидетельствуют о большем видовом разнообразии бактерий, присутствующих в опухолевой микробиоте пациентов с выживаемостью более 5 лет. Эти результаты были подтверждены исследователями во второй когорте.
Иммуномодуляция
Кроме того, авторы подчеркнули, что каждая из двух групп пациентов демонстрировала специфическую сигнатуру внутриопухолевой микробиоты: наличие и высокая численность 3 видов бактерий (Pseudoxanthomonas, Streptomyces, Saccharopolyspora) и Bacillus clausii позволяли прогнозировать выживаемость в 97,51–99,17 % случаев (по данным исследования когорты). Дополнительные иммуногистологические анализы позволяют предположить, что состав микробиоты опухоли может влиять на развитие онкологического заболевания, модулируя противоопухолевый иммунный ответ посредством рекрутирования и активации CD8 Т-клеток.
Связь кишечника и опухоли
Одновременное исследование кала, резецированных опухолевых тканей и окружающих здоровых тканей у трех типов пациентов показал, что микробиота кишечника составляет около 25 % опухолевой микробиоты, притом что она отсутствует в окружающих тканях: таким образом, микробиота опухоли может быть колонизирована микробиотой кишечника. В итоге, трансплантация фекальной микробиоты (ТФМ) от трех типов пациентов (с долгосрочной выживаемостью, краткосрочной выживаемостью или из контрольной группы) была выполнена на мышах. В ходе этих работ подтвердилась способность кишечной микробиоты колонизировать опухоли поджелудочной железы. Они также позволили предположить ее способность модифицировать бактериальный состав опухоли и в свою очередь модулировать иммунную функцию, таким образом влияя на прогрессирование рака и выживаемость пациента. Помимо возможности прогнозирования на основе микробиоты опухоли, результаты ТФМ позволяют надеяться, что однажды мы сможем манипулировать этой микробиотой для повышения прогнозируемой продолжительности жизни пациентов с PDAC, для которых в настоящее время имеется очень мало терапевтических возможностей.