Хотя применение пребиотиков или пробиотиков и трансплантации фекальной микробиоты (ТФМ) имеет ограничения у больных с ослабленным иммунитетом из-за повышенного инфекционного риска, оно может приносить значительную пользу больным, перенесшим ТГСК. Вместе с новыми методами анализа, характеристики и мониторинга микробиоты кишечника, применение этих подходов может положительно влиять на профилактику инфекций и снижать риск отторжения трансплантата.
В исследовании с участием 30 детей и подростков применение пробиотиков, особенно Lactobacillus plantarum, на этапе антибиотикопрофилактики или наблюдения после ТГСК позволило предупредить начало РТПХ в 70 % случаев, при этом без последующей бактериемии, ассоциированной с L. Plantarum13. Продолжаются и другие исследования по снижению частоты реакции отторжения трансплантата на фоне терапии L. rhamnosus GG. Что касается ТФМ, ее безопасность и положительный эффект против инфекции C. difficile были недавно доказаны на небольших группах пациентов, перенесших ТГСК13: в одном исследовании ТФМ привела к ремиссии в 3 из 4 случаев, а в другом исследовании – к ослаблению симптомов РТПХ после нескольких пересадок. Микробиота пациентов, получавших антибиотики, которым проводили трансплантацию аутологичной фекальной микробиоты, восстанавливалась по прошествии чуть более 100 дней с момента ТГСК16. В связи с этим некоторые ученые предлагают выполнять ТФМ перед ТГСК у пациентов-носителей резистентных штаммов C. Difficile.
ПИТАНИЕ И ПРОБИОТИКИ
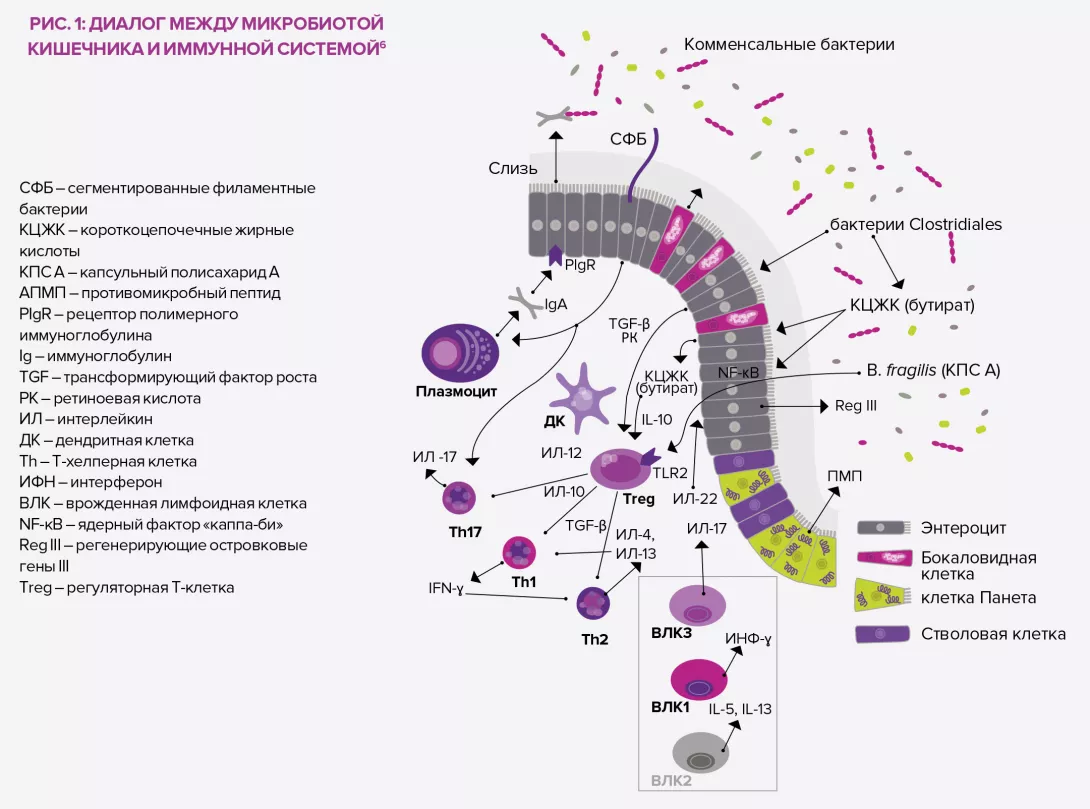
Короткоцепочечные жирные кислоты, такие как бутират, показали положительный эффект в отношении РТПХ. Они служат источником энергии, а также препятствуют апоптозу энтероцитов и обладают противовоспалительным действием, способствуя синтезу регуляторных T-клеток. Наблюдалось благоприятное воздействие на слизистую оболочку кишечника других компонентов, метаболизируемых желудочно-кишечной микробиотой: производных индола, образующихся при ферментативном расщеплении крестоцветных (капуста, брокколи…), триптофана (молочные продукты, бананы17…), желчных кислот. Сочетание пищевых волокон, глютамина и олигосахаридов снизило уровень осложнений и смертности среди 44 пациентов после трансплантации. В настоящее время продолжаются испытания в отношении пользы резистентного крахмала, пребиотика, способствующего выработке бутирата12.
ДРУГИЕ ИННОВАЦИИ НА СТАДИИ РАЗРАБОТКИ
Арсенал терапевтических средств может также расшириться за счет таких инноваций, как направленная антибиотикотерапия, целью которой является сдерживание разрушения пищеварительного барьера и появления бактерий с множественной лекарственной устойчивостью (в настоящее время ведутся испытания антибиотиков на основе патоген-специфических антител и синтетических бактерий, конкурирующими с патогенами). Благодаря новым технологиям мы можем воссоздавать в лабораторных условиях взаимодействия, которые происходят в желудочно-кишечной микробиоте в естественных условиях. Что касается инструментов составления бактериального профиля, они открывают путь к персонализированной медицине, адаптированной к микробиоте каждого пациента, для выбора наиболее подходящего протокола терапии12.