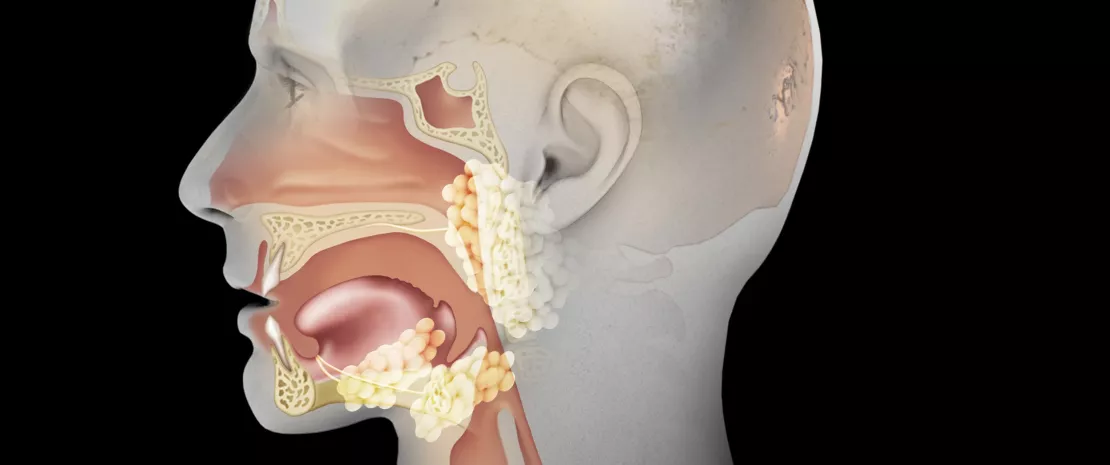
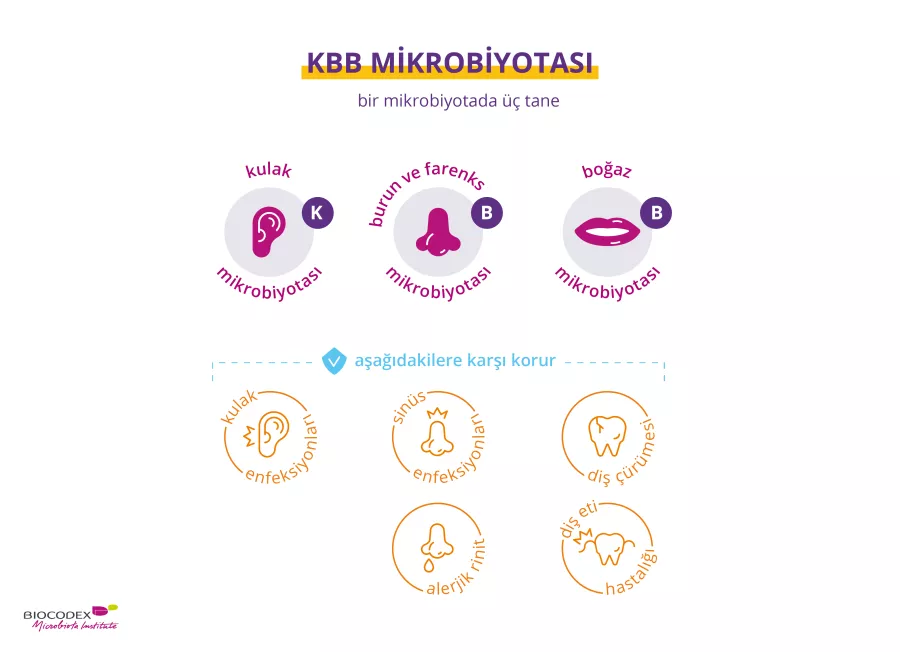
Genelde "Kulak, burun ve boğaz (KBB) mikrobiyotası" olarak adlandırılan mikrobiyota aslında bir değil birkaç mikrobiyotadan oluşur. Antibiyotiklerin, ağız boşluğundan sinüslerin içi ve hatta orta kulak dahil farenkse uzanan bu farklı mikrobiyotalar üzerinde ayrı etki etmesi olasıdır. Bu bölüm asıl olarak mükemmel bir örnek olan Üst Solunum Yolu (ÜSY) mikrobiyotası üzerinde antibiyotiklerin etkilerine ayrılmıştır: ÜSY mikrobiyotası kulak sağlığın koruyucularından biri olarak görünür ancak özellikle akut otitis medya olgularında bu amaçla reçetelendirilmiş antibiyotikler tarafından tehdit altındadır.
ÜYS MİKROBİYOTASI, KULAK SAĞLIĞININ DOSTU MU?
ÜYS mikrobiyotası doğumdan hemen sonra çeşitli konakçı bakteriler tarafından kolonize edilir (Dolosigranulum Corynebacterium, Staphylococcus, Moraxella, Streptococcus). Konakçı türlerin (Dolosigranulum spp. ve Corynebacterium spp.) göreceli olarak daha yüksek sayıda olması ile birlikte nazofarengeal mikrobiyotada1 daha fazla çeşitliliğin, akut otitis media'da (AOM) rolü olduğu gösterilen üç otopatojen olan Streptococcus pneumoniae, Haemophilus influenzae ve Moraxella catarrhalis2,3 tarafından daha düşük ÜYS'in kolonizasyon insidansı ile ilişkilendirildiğine dair artan sayıda kanıt vardır.
ANTİBİYOTİK TEDAVİSİ: AZ FAYDA İÇİN ÇOK RİSK
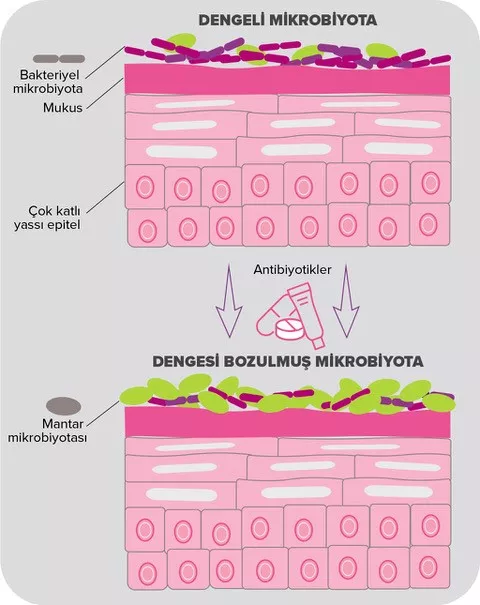
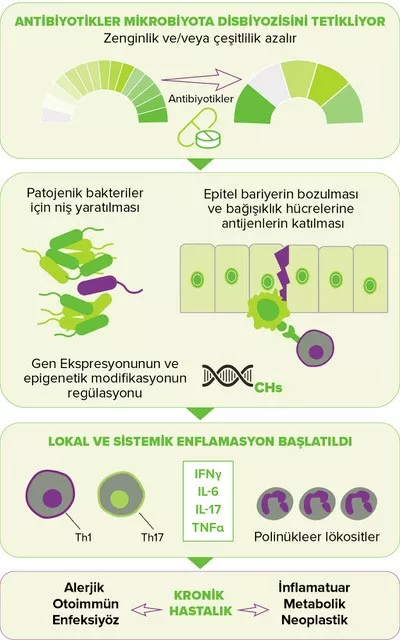
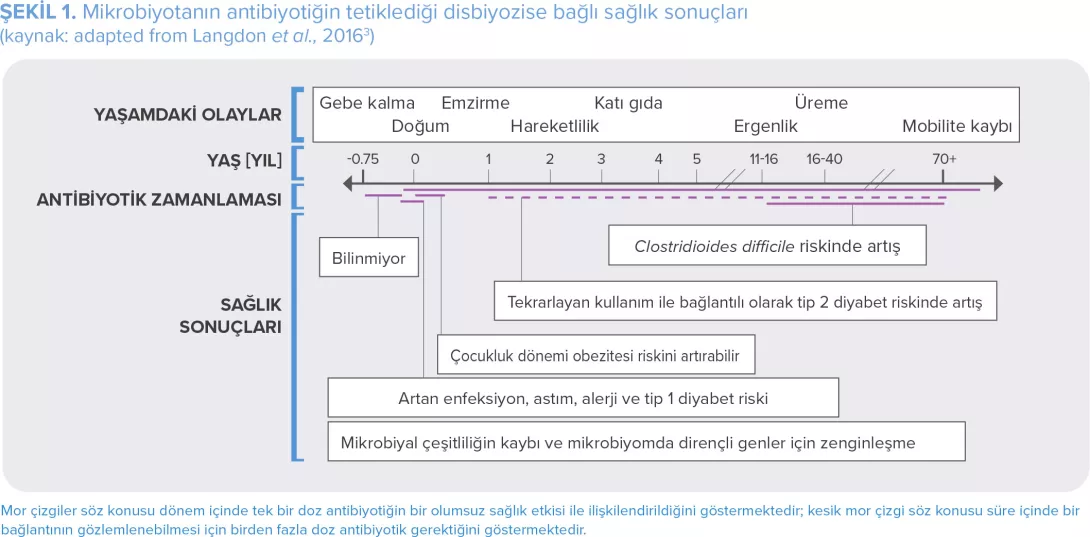
Antibiyotikler maruz kalmak koruyucu türlerin sayısını azaltarak ve Gram-negative bakteriler (Burkholderia spp., Enterobacteriaceae, Comamonadaceae, Bradyrhizobiaceae)4,5, ile birlikte S. pneumoniae, H. influenzae ve M. catarrhalis'in5 sayısını artırarak ÜYS mikrobiyotasına etki eder. Antimikrobiyal Direnç elde etmelerinin sonucu olarak, bu nişte başka şekilde başarılı rekabet edemeyecek bu bakterilere, tedavi sırasında patojenik olabilecek ölçüde çoğalma fırsatı verilir6. Ayrıca antibiyotiklerin pediatrik AOM (çocuklara antibiyotik verilmesinin ana nedeni7) ve diğer ÜSY enfeksiyonları (boğaz ağrısı veya soğuk algınlığı)7,8, olgularının çoğunda, bu hastalıkların çoğunlukla bakteriyel olmayan yapıları nedeniyle herhangi bir fayda sağlamasının olası olmadığı düşünülmektedir: AOM olan çocukların %60 ile %90'ı antibiyotik olmadan iyileşmektedir9,10. Son olarak antibiyotikler, antibiyotik ilişkili diyare gibi yan etkilere neden olabilen bağırsak mikrobiyotasında disbiyozise yol açar3,11 (bkz. sayfa 4: bağırsak mikrobiyotası).