Anatomie féminine, microbiotes et hygiène intime
La différence entre la vulve et le vagin (vous ne comprenez pas ?). L'hygiène intime ? (vous ne comprenez toujours pas ?)... Quand on interroge les femmes sur ces sujets, elles sont souvent évasives. Cours pratique d'anatomie et de bonnes pratiques.

Alors qu’on les croyait libérées par les combats féministes des années 2000, les jeunes générations s’avèrent encore moins à l'aise que leurs aînées quand il s’agit de parler des organes génitaux féminins. Et pendant que les quarantenaires, influencées par des spots publicitaires sur la fraîcheur de l’entrejambe, se ruent sur les déodorants intimes, la génération suivante, attentive à son image, se révèle adepte de procédures esthétiques, comme la (sidenote: Vulvoplastie Chirurgie plastique de la vulve, pour augmenter ou réduire la taille ou le volume des grandes lèvres. ) 1. A chaque génération son lien avec l’intime, donc. Reste que l’hygiène et la santé de cette zone corporelle fragile doivent être une préoccupation de tout âge… d’où quelques rappels (dé ?)culottés, afin de lever le voile sur d’éventuels tabous.

Un peu d'anatomie
L’appareil génital féminin est à la fois une terra incognita en termes d’anatomie et un tabou en termes de conversation, y compris chez les femmes. Tant et si bien que les professionnels de santé peinent à comprendre les maux de leurs patientes faute d’explications claires, et/ou parce qu’elles confondent la vulve (partie externe de leur appareil génital) avec leur vagin (partie interne) 1.
Pour faire court :
la vulve, c’est dehors ; le vagin, c’est dedans !
La vulve
comprend un ensemble de tissus visibles lors d’un examen externe 1 :
- une partie du mont du pubis (ou mont de Vénus), zone charnue et poilue qui recouvre l’os du pubis,
- le clitoris, lié au plaisir sexuel, homologue féminin du prépuce de l’homme,
- les grandes lèvres, plis extérieurs protecteurs,
- les petites lèvres, situées à l’intérieur des grandes lèvres, qui comprennent de nombreuses glandes sébacées,
- et le vestibule vulvaire, zone située entre les petites lèvres où se trouve l'entrée du vagin et, juste au-dessus, le méat urétral (orifice du système urinaire).
La peau du mont du pubis et des grandes lèvres est dotée de glandes sébacées 1 qui produisent un film hydrolipidique protecteur 1,2. La vulve est par ailleurs dotée de glandes (glandes de Bartholin, glandes de Skene) qui assurent la lubrification des petites lèvres et du vestibule vulvaire lors des rapports sexuels 1.
le vagin
D’une dizaine de centimètres de longueur, le vagin est une cavité qui n’est pas visible de l’extérieur.
- Sur sa partie basse, il communique avec l’extérieur au niveau de la vulve, et plus précisément du vestibule vulvaire ;
- à son sommet, il aboutit au col de l’utérus1.
Le vagin peut accueillir les tampons et coupes menstruelles durant les règles, le pénis d’un partenaire lors de rapports sexuels ou votre sextoy préféré… et le speculum de votre gynéco lors de vos rendez-vous médicaux !
Au point où nous en sommes, autant faire le tour de tous les orifices. D’avant en arrière, le sexe féminin comprend, dans l’ordre, trois ouvertures :
- le méat urinaire, relié à la vessie (qui stocke l’urine) par un canal appelé l’urètre (qui permet d'évacuer l'urine à l'extérieur du corps lors de la miction) 2,
- puis l’entrée du vagin (reproduction),
- puis l’anus (selles).
On parle d’ailleurs de :
pour désigner la zone qui entoure l’anus ;
pour désigner le grand ensemble formé par la vulve et la zone péri-anale (autrement dit, tout l’entrejambe) 1.
Les microbiotes de l'intime féminin
Notre intimité ne fait pas exception : comme les autres organes, elle abrite un microbiote ou plutôt des microbiotes avec :
Commençons par le microbiote vulvaire. On aurait pu croire qu’il était connu sur le bout des doigts puisque externe. Et pourtant, force est de reconnaître que les données à son sujet ne sont pas légion 1,3. Les rares études évoquent, du bout des lèvres, la possible présence de bactéries diverses et variées (Lactobacillus, Corynebacterium, Staphylococcus et Prevotella) et de champignons de type levures 1,3.
D’ailleurs, peut-être faudrait-il envisager de parler non pas d’un microbiote vulvaire, mais de microbiotes vulvaires (au pluriel), selon les zones de la vulve : un microbiote du mont du pubis, un microbiote des grandes lèvres, un microbiote des petites lèvres…3.
Une chose semble néanmoins acquise : la diversité est doublement de mise, que ce soit :
au sein du microbiote vulvaire de chaque femme où coexistent foison de
(sidenote:
Microorganismes
Organismes vivants qui sont trop petits pour être vus à l'oeil nu. Ils incluent les bactéries, les virus, les champignons, les archées, les protozoaires, etc… et sont communément appelés "microbes".
Source : What is microbiology? Microbiology Society.
)
,
ou entre deux femmes (aucune espèce commune à toutes les femmes n’est répertoriée) 1.
Du côté du microbiote vaginal (ou flore vaginale), c’est tout le contraire. Dans le vagin, les lactobacilles (notamment Lactobacillus crispatus, Lactobacillus iners, Lactobacillus gasseri et Lactobacillus jensenii) règnent généralement en maîtres et maintiennent une acidité locale grâce à leur production d’acide lactique 1,4.
Ce pH acide, de 4,0 à 4,5, tient à distance les (sidenote: pathogènes Un pathogène est un microorganisme qui cause, ou peut causer, une maladie Pirofski LA, Casadevall A. Q and A: What is a pathogen? A question that begs the point. BMC Biol. 2012 Jan 31;10:6. ) , de même que l’eau oxygénée et les bactériocines produites par ces mêmes lactobacilles pour venir à bout des pathogènes les plus récalcitrants.
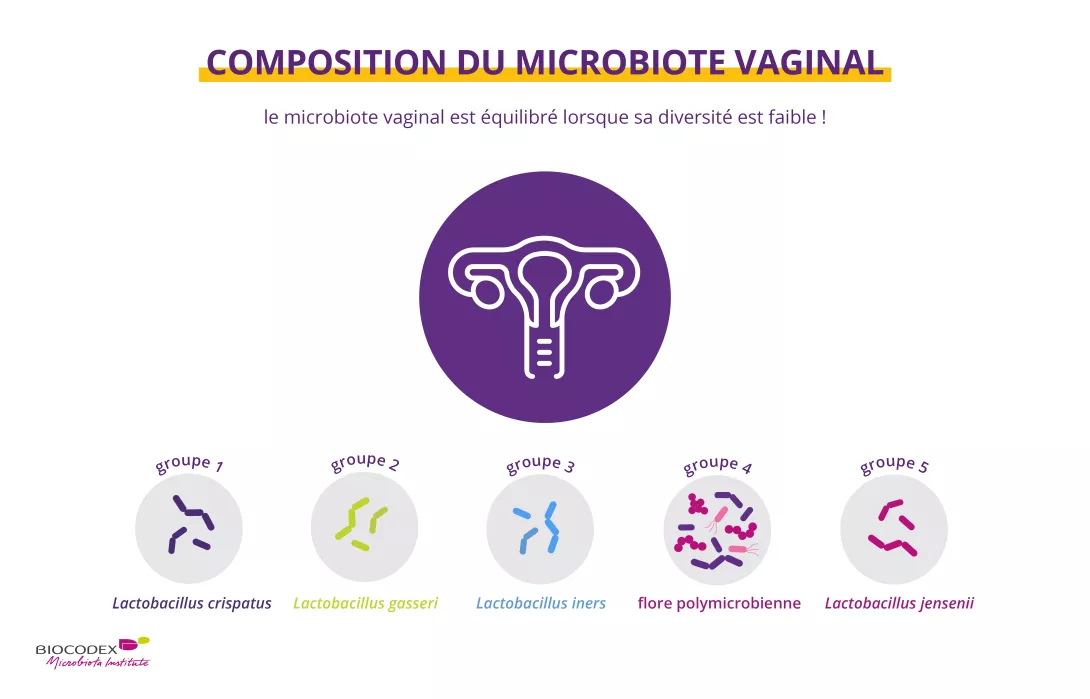
Représentation des principaux groupes de bactéries du microbiote vaginal, dont les lactobacilles, clés de l’équilibre intime et de la prévention des infections
Le microbiote urinaire a longtemps été considéré comme stérile. Une erreur puisque l’urine contenue dans la vessie possède elle aussi un écosystème microbien. Bien que le microbiote urinaire soit bien distinct de ses proches voisins (microbiotes anal, vaginal, ou vulvaire), il partage avec eux certains microorganismes 5. Il est aussi beaucoup moins densement peuplé, et souvent dominé par un seul type bactérien. On retrouve principalement les lactobacilles mais aussi Gardnerella, Streptococcus et Corynebacterium 6.
Enfin, le microbiote périanal est le reflet de notre très riche microbiote intestinal, et notamment colique : lors de l’émission de selles, les bactéries intestinales se retrouvent en contact avec cette zone et peuvent y élire domicile 1.
1 sur 5 Seulement 22 % des femmes déclarent savoir exactement ce qu’est le « microbiote vaginal » (+2 points vs 2023).
Des microbiotes trop proches pour ne pas échanger
Les microbiotes vulvaire, vaginal, et péri-anal évoluent avec le temps. Par exemple, le microbiote vaginal est sous l’influence de l’âge, des hormones sexuelles et de facteurs extérieurs comme la pollution, le stress, les antibiotiques, etc. 4 Des déséquilibres peuvent apparaître : après la ménopause, la chute des œstrogènes induit une perte de lactobacilles et donc une hausse du pH, avec à la clé de fréquentes dysbioses vaginales 7. Le microbiote anal dépend quant à lui surtout de l’alimentation et du stress : un excès d’anxiété induit une réponse inflammatoire qui favorise le développement de bactéries pathogènes dans le tube digestif… qui terminent leur course dans la zone périanale 1.
En parallèle, la proximité des orifices urinaire, vaginal et anal explique de possibles « échanges » de flore entre les 3 microbiotes de ces 3 zones… et la possible invasion du microbiote vaginal par des Escherichia coli digestives par exemple, qui se seraient aventurées au-delà de la zone péri-anale 1.
Vaginose Bactérienne
Antibiotiques

Hyper-hygiène, sur-épilation et vêtement trop serrés : le combo perdant
Parfois, ce sont paradoxalement des pratiques d’hygiène intime inadaptées qui favorisent les échanges et ou des déséquilibres. Un lavage trop agressif (produits inadaptés) ou trop fréquent (plus d’une fois par jour) de la vulve peut rapidement mettre à mal la fonction barrière de la peau de cette zone, très fragile et très réactive. L’eau seule peut suffire à l’assécher et à l’exposer à des démangeaisons et brûlures 8. Quant aux savons parfumés, sprays hygiéniques, lubrifiants, déodorants… que certaines s’auto-prescrivent pour tenter de traiter les odeurs, démangeaisons, douleurs et sécheresses, ils sont contre-productifs 4.
A proscrire également :
Les produits non destinés à la toilette intime (désinfectants pour les mains, lingettes pour bébé, huiles, crème à raser et lotions pour le corps). Ces derniers sont détournés de leur usage premier par plus de femmes que l’on ne le pense : 41,6 % des femmes d’une étude reconnaissent avoir utilisé des lingettes pour bébé pour leur toilette vulvaire… et 2,1 % pour une toilette vaginale interne 4 !
Et rappelons-le au passage :
le vagin n’a aucunement besoin d’être nettoyé.
Autre erreur récurrente : l’épilation ou le rasage total de la vulve 1,9. Un phénomène de mode qui concerne 84 % des Américaines préménopausées, pour 2/3 desquelles il s’agit d’une routine quotidienne ou hebdomadaire. Souvent justifié par des raisons d’hygiène, elle est tout au contraire associée avec des lésions qui facilitent l’entrée de bactéries ou de virus. D’ailleurs, on observerait une altération du microbiote vaginal chez les femmes qui décident d’une épilation totale de leur vulve 9.
Enfin, le port de vêtements très serrés et synthétique semble favoriser le développement de pathogènes (environnement plus humide et chaud), avec à la clé des démangeaisons et des problèmes urogénitaux plus fréquents 1.

Bonnes pratiques pour préserver le microbiote vaginal : toilette intime douce, prébiotiques et probiotiques – à l'inverse des douches vaginales, savons agressifs et solutions antiseptiques.

Mieux informer les femmes
1 sur 2 52 % des femmes interrogées déclarent n’avoir jamais reçu des informations sur les bons gestes de toilette intime et 25 % n’avoir été informées qu’à une seule reprise par leur praticien de santé.
Pourquoi un tel décalage entre les pratiques et les recommandations ? Les raisons sont sans doute multiples :
- trop peu de femmes sont informées par leur médecin sur les bons gestes : 52 % des femmes interrogées déclarent n’avoir jamais reçu de telles informations et 25 % n’avoir été informées qu’à une seule reprise par leur praticien de santé ;
- la confusion fréquente entre vulve et vagin entretient la mauvaise compréhension des messages ;
- les mythes les plus stupides sont souvent les plus tenaces 1.
L’enjeu est d’autant plus important que la vulve est la première ligne de défense du système génital des femmes 10.
Ce que les femmes savent (et ignorent) de leur microbiote vaginal

Les (vraies !) bonnes pratiques d’hygiène
Les bons gestes pour préserver le microbiote et le délicat film hydrolipidique protecteur du sexe féminin ? Une routine qui respecte l’équilibre de la vulve et des soins adaptés à l’âge et aux spécificités de chaque femme.
Avec dans tous les cas 3 grands principes immuables 10 :
- un lavage externe uniquement (= de la vulve, pas de douche vaginale), d’avant en arrière (la vulve puis l’anus)
- sans gant de toilette (susceptible de contenir des bactéries) mais avec vos mains préalablement lavées,
- une fois par jour. Seules les femmes souffrant de diarrhées fréquentes peuvent justifier un lavage externe plus fréquent (du fait des selles plus fréquentes). Idem en période de règles où il est éventuellement possible de procéder à une seconde toilette intime dans la journée.
Le lavage à l'eau uniquement peut dessécher la peau et aggraver les démangeaisons 10. Il convient de privilégier un soin lavant doux, sans savon, qui respecte le microenvironnement vulvaire et maintient l’équilibre de son microbiote 1. Et c’est tout. Soyez intimement convaincue que, sur cette délicate zone corporelle, le mieux est l’ennemi du bien.
Enfin, quelques autres recommandations vous aideront à adopter les bons gestes tout au long de la journée 10 :
- la nuit, évitez les sous-vêtements ;
- au sortir de la douche (à préférer au bain), séchez–vous soigneusement avec votre serviette personnelle, sans frotter mais en tamponnant doucement votre entrejambe ;
- lorsque vous vous habillez, optez pour des sous-vêtements en coton plutôt qu’en matière synthétique, évitez l’usage régulier de protèges slip, privilégiez les vêtements amples, remplacez si possible vos collants par des bas ;
- aux toilettes, essuyez-vous d’avant en arrière (pour ne pas ramener des bactéries anales vers la vulve) avec un papier non parfumé et idéalement non coloré ;
- encore une fois on garde les grands principes de la toilette intime (lavage externe uniquement ; avec vos mains ; une fois par jour… ) 10
- après des relations sexuelles (protégées !, tant que vous ne savez pas si votre partenaire peut être porteur d’une IST), prenez soin d’uriner si vous êtes sujette aux cystites ;
- en période de règles, n’utilisez pas de protections périodiques parfumées et changez régulièrement votre protection ou tampon. 10

Probiotiques et prébiotiques
La bonne santé du microbiote vaginal repose sur une bonne hygiène intime. Mais parfois, cela ne suffit pas et un petit coup de pouce peut s’avérer nécessaire pour re-doper les bonnes bactéries de notre microbiote, avec :
Probiotiques
Des probiotiques, micro-organismes vivants qui, lorsqu’ils sont administrés en quantité appropriée, produisent des effets bénéfiques sur la santé de l’hôte 11,12. Administrés par voie orale ou vaginale, ils peuvent contribuer à restaurer la flore vaginale, à améliorer les symptômes et à réduire le risque de récidive de différentes infections vaginales, et ce de la puberté à la ménopause 13.
Prébiotiques
Des prébiotiques, fibres alimentaires non digestibles qui exercent des effets positifs sur la santé et qui sont utilisés de manière sélective par les microorganismes bénéfiques du microbiote de l’hôte 12, 14. Ou pour faire plus court, les aliments préférés des probiotiques qui vont favoriser leur développement. Ainsi, les prébiotiques féminins boostent les lactobacilles vaginaux et participent à la normalisation de l’acidité vaginale 15,16.
Quelle est la différence entre les prébiotiques, les probiotiques et les postbiotiques ?
Pour résumer...
Les organes génitaux féminins sont constitués de :
- la vulve (partie externe)
- et le vagin (cavité qui relie la vulve à l’utérus, dans laquelle vous pouvez introduire un tampon lorsque vous avez vos règles).
Il abrite plusieurs microbiotes : un microbiote vulvaire où la diversité est de mise, un microbiote vaginal largement dominé par les lactobacilles, un microbiote urinaire peu densément peuplé (on a longtemps pensé, à tort, que l’urine était stérile) et un microbiote péri-anal très riche (contact avec les selles).
La proximité des orifices urinaire, vaginal et anal explique de possibles « échanges » de flore entre les microbiotes de ces zones, d’autant plus en cas d’hygiène intime inadaptée : lavage trop agressif, épilation ou rasage total, port de vêtements trop serrés…
Faute d’être informées, beaucoup de femmes n’ont pas adopté les bons gestes pour protéger leurs microbiotes. Mais il n’est pas trop tard : osez en parler avec votre médecin !
Si votre microbiote vaginal est en berne, des prébiotiques et probiotiques peuvent vous aider à restaurer une flore vaginale équilibrée.
2. Biology of the Kidneys and Urinary Tract. MSD Manuel. https://www.msdmanuals.com/home/kidney-and-urinary-tract-disorders/biology-of-the-kidneys-and-urinary-tract
6. Mueller ER, Wolfe AJ, Brubaker L. Female urinary microbiota. Curr Opin Urol. 2017 May;27(3):282-286.
7. Auriemma RS, Scairati R, Del Vecchio G et al. The Vaginal Microbiome: A Long Urogenital Colonization Throughout Woman Life. Front Cell Infect Microbiol. 2021 Jul 6;11:686167.