Les clés d'une consultation réussie par Alessandra Graziottin
Microbiote intestinal et troubles du sommeil : vers une approche thérapeutique basée sur la modulation microbienne ?
Des recherches montrent que le microbiote intestinal influence le sommeil en modulant la production de butyrate, un métabolite qui affecte l'activité neuronale dans l'hypothalamus. De quoi ouvrir la voie à des traitements basés sur l'équilibre bactérien ?
 Des bactéries intestinales en cause dans l’apnée du sommeil
Des bactéries intestinales en cause dans l’apnée du sommeil
 Insomnie du senior : un lien avec le microbiote intestinal
Insomnie du senior : un lien avec le microbiote intestinal
Le secret d'un bon sommeil est dans vos intestins !
Et si la clé d’un sommeil réparateur se cachait dans notre intestin ? Pour bien dormir, il ne suffirait plus seulement de compter les moutons, mais aussi de veiller sur nos bactéries intestinales, histoire de valider que l’on possède bien un microbiote de bon dormeur.
Le microbiote intestinal Les probiotiques
 Apnée du sommeil : des bactéries du microbiote intestinal mises en cause
Apnée du sommeil : des bactéries du microbiote intestinal mises en cause
 Insomnie chez les personnes âgées : le microbiote intestinal impliqué ?
Insomnie chez les personnes âgées : le microbiote intestinal impliqué ?
Diversité ou fonction : qu'est-ce qui définit un microbiote sain ?
Nous abritons en nous une communauté microbienne complexe, le microbiote intestinal, qui a un impact considérable sur notre santé. C'est le siège de processus métaboliques cruciaux influencés par notre alimentation, notre âge et notre environnement. Sa force ne s'appuie pas seulement sur la variété des microbes, mais aussi sur les fonctions essentielles qu'ils remplissent ensemble. Étant donné qu'un état sain est un équilibre dynamique entre nous et ces microbes, qu'est-ce qui définit un microbiote sain ?
 De la ferme à l’intestin : les étonnants effets des fruits et légumes sur le microbiote intestinal
De la ferme à l’intestin : les étonnants effets des fruits et légumes sur le microbiote intestinal
 Tout ce que vous devez savoir sur la dysbiose
Tout ce que vous devez savoir sur la dysbiose
Au-delà de la diversité : percer les secrets d'un microbiote intestinal sain
La vision conventionnelle d'un intestin sain a longtemps été dominée par l'idée que la diversité était reine. On pensait qu'une grande variété d'espèces microbiennes était le principal indicateur d'un bon fonctionnement de l'intestin. Cependant, nos sources suggèrent que cela est beaucoup trop simpliste. Alors, qu'est-ce qui définit un « microbiote sain » ?
Le microbiote intestinal Prébiotiques : l'essentiel pour comprendre Troubles digestifs L'alimentation
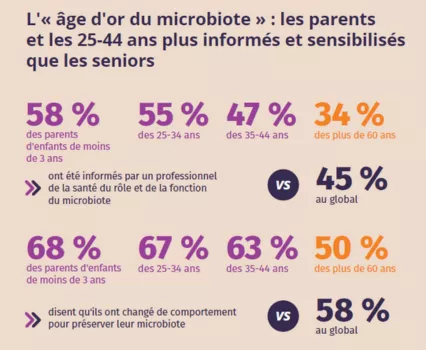
Observatoire international des microbiotes 2nd édition
Par Biocodex Microbiota Institute et IPSOS
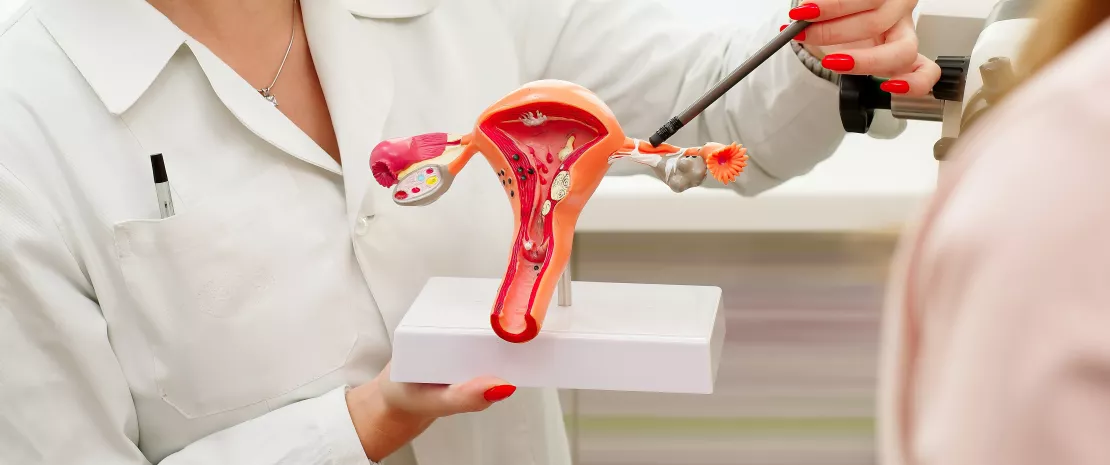
Microbiote vaginal #22
Par la Pr. Satu. Pekkala
Chercheuse à l’Académie de Finlande, Faculté des sciences
du sport et de la santé, Université de Jyväskylä, Finlande