БАКТЕРИАЛЬНЫЙ ВАГИНОЗ
Бактериальный вагиноз — самое распространенное гинекологическое заболевание, которым страдают 23–29% женщин детородного возраста во всем мире.1 Болезнь ведет себя по-разному: она может протекать бессимптомно, но может доставлять и серьезные неудобства. Причина возникновения бактериального вагиноза остается неизвестной, но наиболее вероятным объяснением является дисбаланс микробиоты влагалища.2

Что такое бактериальный вагиноз?
Бактериальный вагиноз — потенциально опасное и сложно диагностируемое заболевание. 50% женщин переносят его бессимптомно, в то время как остальные страдают от местного раздражения или неприятного запаха.
Для диагностики бактериального вагиноза практикующие врачи используют критерии Амселя. Диагноз основан на наличии по крайней мере трех из следующих критериев:
- жидкие, гомогенные выделения из влагалища;
- pH влагалища выше 4,5;
- запах амина (похожий на запах рыбы) после проведения специального теста на материале вагинального мазка;
- наличие клеток эпителия влагалища, покрытых бактериями, при микроскопическом исследовании выделений.
С этим заболеванием связаны многие факторы риска, включая возраст, менструальный цикл, беременность, сексуальный анамнез, а также спринцевание и курение.3 Вагинальный дисбиоз, вызванный применением антибиотиков, также может способствовать развитию бактериального вагиноза, создавая порочный круг, поскольку антибиотики используются для лечения инфекции.3
Наконец, женщины с бактериальным вагинозом чаще заражаются инфекциями, передаваемыми половым путем (ИППП), включая герпес, ВПЧ, СПИД и бактериальные инфекции.5,6
50% женщин переносят его бессимптомно, в то время как остальные страдают от местного раздражения или неприятного запаха
Есть ли связь с микробиотой влагалища?
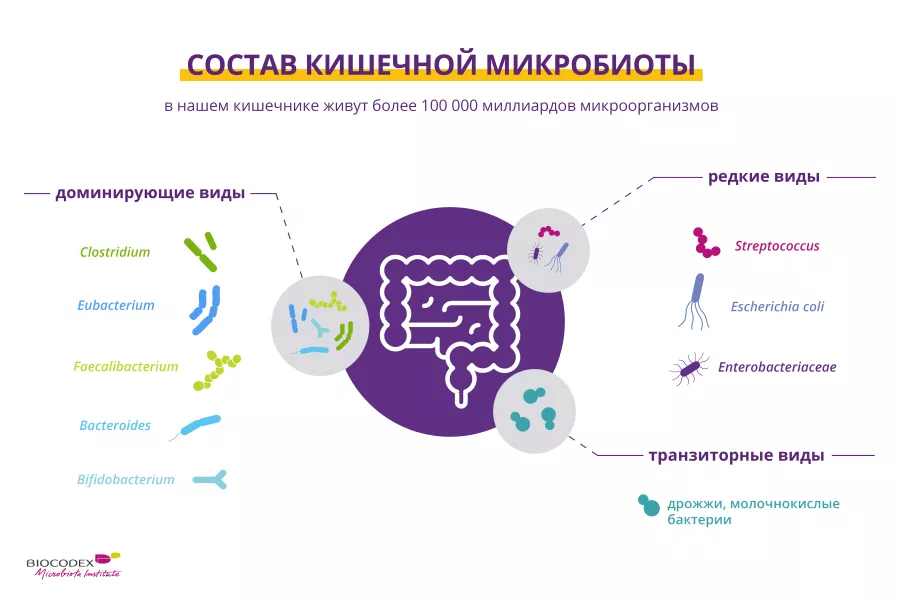
Развитие бактериального вагиноза связано с дисбалансом ( (sidenote: Дисбиоз Изменение состава и функции микробиоты, вызванное сочетанием экологических и индивидуальных факторов. Дисбиоз не является четко очерченным состоянием и варьируется в зависимости от состояния здоровья каждого человека. Levy M, Kolodziejczyk AA, Thaiss CA, et al. Dysbiosis and the immune system. Nat Rev Immunol. 2017;17(4):219-232. ) ) микробиоты влагалища.2 В микробиоте влагалища преобладают различные виды бактерий рода (sidenote: Лактобактерии Палочковидные бактерии, основным свойством которых является производство молочной кислоты, в связи с чем их еще называют «молочнокислые бактерии». Лактобактерии присутствуют в микробиоте полости рта, влагалища и кишечника человека, а также в организме животных и в растениях. Они содержатся в ферментированных продуктах — сырах, йогуртах, соленых огурцах, квашеной капусте и т. д. Лактобактерии также содержатся в пробиотиках, причем своими полезными свойствами пробиотики обязаны именно некоторым видам лактобактерий. W. H. Holzapfel et B. J. Wood, The Genera of Lactic Acid Bacteria, 2, Springer-Verlag, 1st ed. 1995 (2012), 411 p. « The genus Lactobacillus par W. P. Hammes, R. F. Vogel Tannock GW. A special fondness for lactobacilli. Appl Environ Microbiol. 2004 Jun;70(6):3189-94. Smith TJ, Rigassio-Radler D, Denmark R, et al. Effect of Lactobacillus rhamnosus LGG® and Bifidobacterium animalis ssp. lactis BB-12® on health-related quality of life in college students affected by upper respiratory infections. Br J Nutr. 2013 Jun;109(11):1999-2007. ) (sidenote: Лактобактерии Палочковидные бактерии, основным свойством которых является производство молочной кислоты, в связи с чем их еще называют «молочнокислые бактерии». Лактобактерии присутствуют в микробиоте полости рта, влагалища и кишечника человека, а также в организме животных и в растениях. Они содержатся в ферментированных продуктах — сырах, йогуртах, соленых огурцах, квашеной капусте и т. д. Лактобактерии также содержатся в пробиотиках, причем своими полезными свойствами пробиотики обязаны именно некоторым видам лактобактерий. W. H. Holzapfel et B. J. Wood, The Genera of Lactic Acid Bacteria, 2, Springer-Verlag, 1st ed. 1995 (2012), 411 p. « The genus Lactobacillus par W. P. Hammes, R. F. Vogel Tannock GW. A special fondness for lactobacilli. Appl Environ Microbiol. 2004 Jun;70(6):3189-94. Smith TJ, Rigassio-Radler D, Denmark R, et al. Effect of Lactobacillus rhamnosus LGG® and Bifidobacterium animalis ssp. lactis BB-12® on health-related quality of life in college students affected by upper respiratory infections. Br J Nutr. 2013 Jun;109(11):1999-2007. ) Эти бактерии помогают поддерживать во влагалище кислую среду (рН), таким образом предотвращая размножение патогенных бактерий. В микробиоте влагалища также содержится небольшое количество дрожжей, таких как Candida albicans.8
При бактериальном вагинозе нормальная микробная флора заменяется флорой полимикробной, которая содержит различные бактерии (Gardnerella, Atopobium, Prevotella, Mobiluncus и др.).2 Это приводит к снижению преобладания видов Lactobacillus и повышению рН влагалища (среда которого обычно - резко кислая). Однако, только наличие видов бактерий из этой полимикробной флоры, по-видимому, не является причиной инфекции, то есть женщина, во влагалище которой присутствуют виды Atopobium или Prevotella, не обязательно отметит у себя симптомы заболевания. На самом деле Gardnerella vaginalis присутствует у 90% пациенток с симптомами и у 45% здоровых женщин.4 Долгое время эту бактерию считали основным возбудителем бактериального вагиноза, однако новые исследования показали, что Gardnerella vaginalis способна колонизировать влагалище, не вызывая инфекции. Исследования в этой области продолжаются, и причины инфекции еще предстоит установить.3
35% только 1 из 3 женщин знает, что бактериальный вагиноз связан с дисбалансом вагинальной микробиоты
Как избежать бактериального вагиноза
Лечение рекомендуется только для женщин с симптомами. Оно включает в себя назначение пероральных или вагинальных антибиотиков.2 Хотя антибиотики могут помочь облегчить симптомы, к сожалению, болезнь очень часто рецидивирует.11
Тем не менее, есть ряд способов снизить риск развития бактериального вагиноза. Во-первых, следует избегать некоторых факторов риска, таких как спринцевание и курение.3 Для лечения или предотвращения рецидивов можно использовать вагинальные или пероральные пробиотики,12,13 которые восстанавливают баланс микробиоты влагалища.
Эта статья основана на информации, полученной из официальных научных источников, однако она не заменяет собой консультацию медицинского специалиста. При возникновении симптомов проконсультируйтесь с семейным врачом или гинекологом.
1 Peebles K, Velloza J, Balkus JE, et al. High Global Burden and Costs of Bacterial Vaginosis: A Systematic Review and Meta-Analysis. Sex Transm Dis. 2019 May;46(5):304-311.
2 Chen X, Lu Y, Chen T, et al. The Female Vaginal Microbiome in Health and Bacterial Vaginosis. Front Cell Infect Microbiol. 2021 Apr 7;11:631972.
3 Coudray MS, Madhivanan P. Bacterial vaginosis-A brief synopsis of the literature. Eur J Obstet Gynecol Reprod Biol. 2019 Dec 24;245:143-148
4 Onderdonk AB, Delaney ML, Fichorova RN. The Human Microbiome during Bacterial Vaginosis. Clin Microbiol Rev. 2016 Apr;29(2):223-38.
5 Lewis FM, Bernstein KT, Aral SO. Vaginal Microbiome and Its Relationship to Behavior, Sexual Health, and Sexually Transmitted Diseases. Obstet Gynecol. 2017;129(4):643-654.
6 Torcia MG. Interplay among Vaginal Microbiome, Immune Response and Sexually Transmitted Viral Infections. Int J Mol Sci. 2019;20(2):266.
7 Greenbaum S, Greenbaum G, Moran-Gilad J, et al. Ecological dynamics of the vaginal microbiome in relation to health and disease. Am J Obstet Gynecol. 2019 Apr;220(4):324-335.
8 d'Enfert C, Kaune AK, Alaban LR, et al. The impact of the Fungus-Host-Microbiota interplay upon Candida albicans infections: current knowledge and new perspectives. FEMS Microbiol Rev. 2020 Nov 24:fuaa060.
10 Muzny CA, Taylor CM, Swords WE, et al. An Updated Conceptual Model on the Pathogenesis of Bacterial Vaginosis. J Infect Dis. 2019 Sep 26;220(9):1399-1405.
11 Bradshaw CS, Brotman RM. Making inroads into improving treatment of bacterial vaginosis - striving for long-term cure. BMC Infect Dis. 2015 Jul 29;15:292.
12 López-Moreno A, Aguilera M. Vaginal Probiotics for Reproductive Health and Related Dysbiosis: Systematic Review and Meta-Analysis. J Clin Med. 2021 Apr 2;10(7):1461.
13 Koirala R, Gargari G, Arioli S, et al. Effect of oral consumption of capsules containing Lactobacillus paracasei LPC-S01 on the vaginal microbiota of healthy adult women: a randomized, placebo-controlled, double-blind crossover study. FEMS Microbiol Ecol. 2020 Jun 1;96(6):fiaa084.