Que sait-on déjà à ce sujet ?
Les troubles déficit de l’attention avec hyperactivité (TDAH) et les troubles du spectre de l’autisme (TSA) sont des troubles du neurodéveloppement. Ces enfants avec TDAH et TSA ont souvent des troubles digestifs à type de douleurs abdominales et constipation. Des anomalies génétiques sont impliquées dans la survenue de ces troubles, en interaction avec des facteurs de risque environnementaux, notamment alimentaire. Ainsi, à côté des traitements médicamenteux, des prises en charge diététiques sont proposées. En effet, la composition du microbiote intestinal est essentielle dans la régulation de l’axe intestin-cerveau. Or, on sait que les enfants avec TSA ont souvent une sélectivité alimentaire qui peut expliquer une modification du microbiote intestinal. En plus de la dysbiose, une augmentation de la perméabilité intestinale a été décrite, de même qu’une inflammation systémique de bas grade, à la fois dans les TDAH et TSA. L’objectif de cette étude était d’analyser en parallèle les modifications du microbiote intestinal dans des groupes TDAH, TSA et ayant à la fois TDAH/TSA, ainsi que chez des fratries non affectées et des témoins non apparentés. Les objectifs secondaires étaient d’évaluer la perméabilité intestinale et le système immunitaire.
Quels sont les principaux résultats apportés par cette étude ?
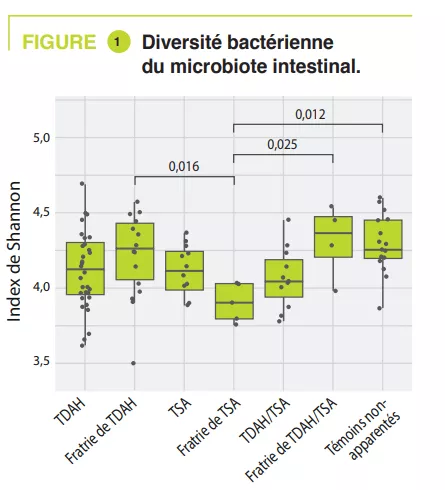
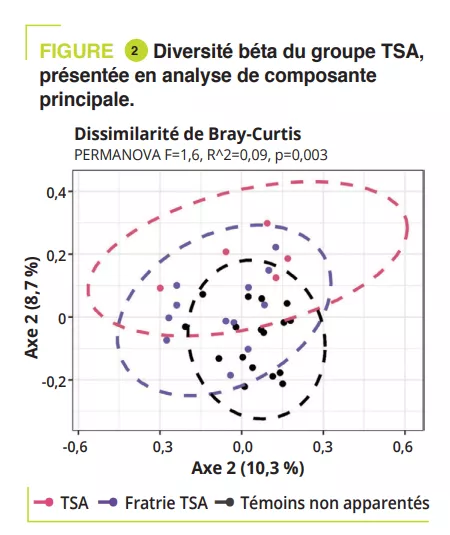
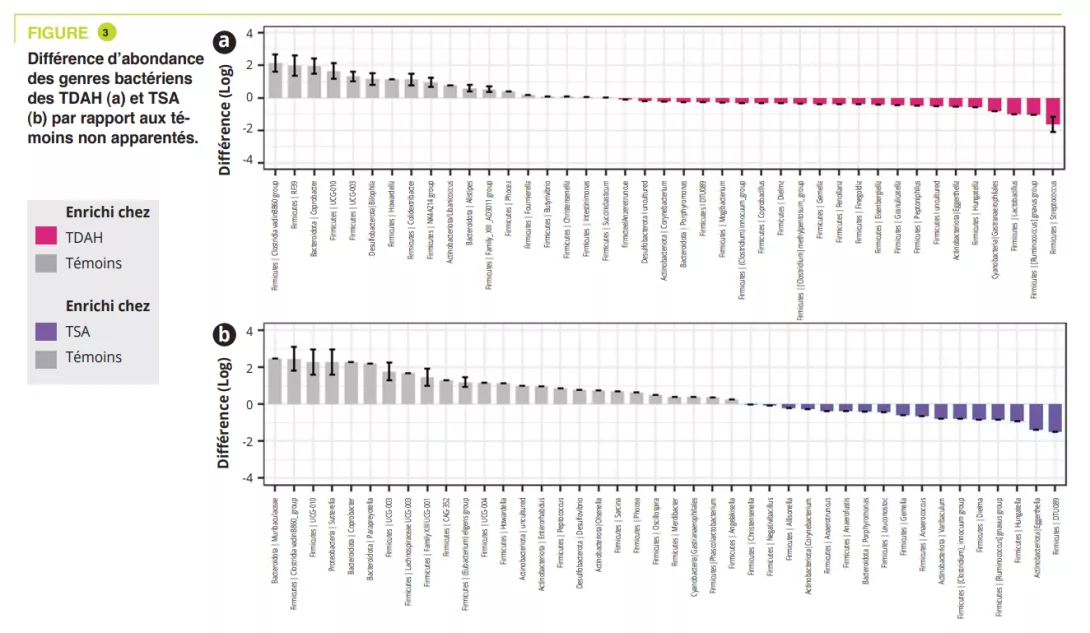
Ont été inclus 95 enfants âgés de 5-17 ans, dont 32 TDAH, 12 TSA, 11 TDAH/ TSA, fratries respectivement 14, 5, 4, et 17 témoins non apparentés. Les troubles digestifs étaient constipation : TDAH 15,6 % (fratrie 7,1 %), TSA 8,3 % (fratrie 0 %), TDAH/TSA 18,2 % (fratrie 0 %), témoins 5,9 % ; douleurs abdominales : TDAH 3,1 % (fratrie 0 %), TSA 16,7 % (fratrie 0 %), TDAH/TSA 18,2 % (fratrie 0 %), témoins 0 % ; et moins souvent un reflux gastro-œsophagien. Une alimentation atypique était retrouvée essentiellement chez les TSA (50 %), marquée par une alimentation peu variée. L’analyse du microbiote intestinal n’a pas retrouvé de variation de la diversité alpha entre TDAH, TSA, TDAH/TSA et témoins apparentés ou non ; par contre, elle était significativement plus faible chez es fratries de TSA (figure 1). La composition du microbiote intestinal était très similaire entre TDAH et TSA, comme en témoigne la diversité béta, mais celle-ci différait significativement entre TDAH et TSA par rapport aux témoins non-apparentés (figure 2). L’analyse de la composition du microbiote intestinal a montré que certains enfants TDAH, TSA, ou TDAH/ TSA avaient une abondance relative plus faible du phylum Bacteroidetes et plus importante d’Actinetobacteria. Tous les groupes étaient dominés par les genres Bacteroides, Faecalibacterium, Blautia et Bifidobacterium ; certains enfants avaient une quantité élevée de Prevotella. Des différences d’abondance des genres bactériens ont été retrouvées entre TDAH, TSA et témoins (figure 3) mais pas entre TDAH et TSA.
Il n’y avait pas de différence de calprotectine fécale entre les différents groupes, ainsi qu’avec les témoins apparentés ou non, de même que pour LPS-binding protéine (LBP). Toutefois, il n’y avait pas de corrélation non plus entre calprotectine fécale et LBP avec les diversités bactériennes alpha et béta. Différentes cytokines et chimiokines ont été mesurées, sans différences significatives entre les différents groupes ; cependant, plusieurs individus TDAH et TSA avaient des taux plus élevés d’IL1-RA par rapport aux témoins non apparentés et 5 enfants TDAH et 1 TSA avaient des concentrations d’IFN-g plus élevées que les témoins non apparentés. Enfin, de faibles corrélations positives ont été trouvées entre LBP et IL-8 (p = 0,023), IL-12 (p = 0,018), IL-13 (p = 0,035) et PlGF (p = 0,045), suggérant qu’une altération de la fonction de barrière intestinale entraînerait une dérégulation immunitaire.
Quelles sont les conséquences en pratique ?
Cette étude a été réalisée sur un petit nombre de personnes, notamment pour les témoins apparentés. Le microbiote intestinal, ainsi que la perméabilité intestinale, pourraient être des cibles pertinentes pour la prise en charge d’enfants et d’adolescents ayant des TDAH et des TSA

 Le microbiote, la clé du diagnostic précoce de la Maladie d'Alzheimer ?
Le microbiote, la clé du diagnostic précoce de la Maladie d'Alzheimer ?
 Le microbiote intestinal, nouveau secret de jouvence ?
Le microbiote intestinal, nouveau secret de jouvence ?