O QUE É QUE JÁ SABEMOS SOBRE ISTO?
O leite materno (LM) é reconhecido como a melhor escolha para alimentar os recém-nascidos, particularmente os bebés de muito baixo peso à nascença (TFPN) com peso inferior a 1250g. Nas unidades de cuidados intensivos, quando o aleitamento materno não é possível, recomenda-se que o leite materno pasteurizado (LFP) seja doado através de um lactário. Além disso, o enriquecimento do LM ou do LFP é muitas vezes necessário para garantir um crescimento ótimo. Este enriquecimento é tradicionalmente efetuado com fortificantes derivados do leite de vaca (FoLV) e, mais recentemente, com fortificantes derivados do leite de mulher (FoLF). Para além disso, sabemos que os recém-nascidos com TFPN têm uma microbiota intestinal anormal. No entanto, não se sabe como é que a composição desta microbiota intestinal pode ser melhorada com os nutrientes utilizados nos fetos com TFPN.
São necessários estudos clínicos para determinar o impacto destes diferentes enriquecimentos na microbiota intestinal dos recém-nascidos com TFPN.
QUAIS SÃO AS PRINCIPAIS CONCLUSÕES DESTE ESTUDO?
O ensaio randomizado controlado OptiMom incluiu 119 recém-nascidos com um peso de nascimento <1250g, 56 FoLV e 63 FoLF. A mediana do termo e do peso ao nascer foi de 880 g e 27,9 semanas, sem diferenças nos vários parâmetros entre os dois grupos.
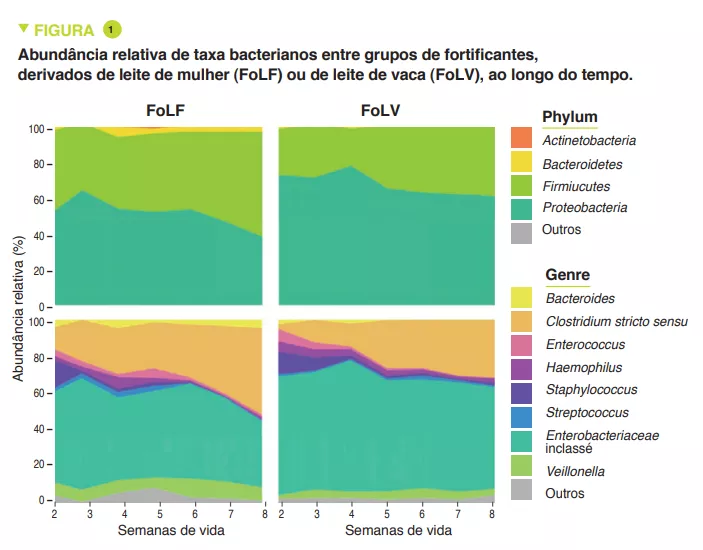
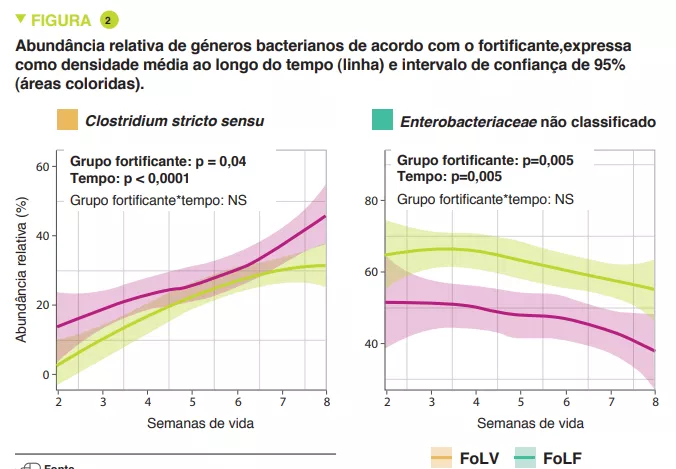
Os recém-nascidos FoLF apresentaram menor diversidade microbiana (índice de Shannon) (p < 0,005). Proteobactérias e Firmicutes predominaram em ambos os grupos, com uma maior abundância relativa de Proteobactérias (p = 0,0003) incluindo Enterobacteriaceae sem classificação (p = 0,005) e uma menor abundância relativa de Firmicutes (p = 0,001) incluindo Clostridium stricto sensu (p = 0,04) em FoLF do que FoLV (Figura 1). A abundância bacteriana aumentou de forma constante ao longo do tempo no grupo FoLV, ao passo que se alterou pouco no grupo FoLF (p = 0,03). A abundância relativa de Clostridium stricto sensu (p = 0,04) foi maior nos recém-nascidos FoLV do que nos FoLF e a de Enterobacteriaceae sem classificação menor (p = 0,005) (Figura 2). Após a normalização da abundância dos taxa, surgiram mais diferenças ao nível do género, com concentrações mais elevadas de Eubacteriaceae sem classificação (p < 0,0001), Streptococcus (p = 0,0002) e Staphylococcus (p = 0,002), e mais baixas de Clostridium stricto sensu (p = 0,04) em recém-nascidos FoLF em comparação com FoLV. Estas alterações na abundância bacteriana estavam associadas a alterações na função microbiana. Por último, foi possível prever o tipo de fortificante recebido com base na abundância microbiana das fezes.
Os autores analisaram os efeitos dos volumes de leite. Em ambos os grupos, volumes mais elevados de LM durante 3 dias foram associados a uma maior diversidade alfa, mas sem relação com a densidade bacteriana total. Com maiores volumes de LM, observou-se uma maior abundância relativa e normalizada de Veillonella em ambos os grupos, e de Streptococcus no grupo FoLV. Foi encontrada uma relação positiva entre os volumes de LM e as concentrações de Staphylococcus no grupo FoLF, e com Eubacteriaceae sem classificação no grupo FoLV.
Os volumes de LFP foram associados a uma maior diversidade apenas no grupo FoLV, tal como a densidade bacteriana. Abundâncias relativas e normalizadas mais baixas de Eubacteriaceae sem classificação, Streptococcus e mais altas de Clostridium stricto senso foram encontradas de forma semelhante em recém-nascidos FoLV com volumes LFP mais altos.
Volumes mais altos de FoLV foram positivamente relacionados à diversidade e densidade bacteriana para o grupo FoLV, mas não para FoLF. Os volumes FoLV foram positivamente associados às abundâncias relativas e normalizadas de Firmicutes e Clostridium stricto sensu, enquanto os volumes FoLF foram positivamente associados às abundâncias relativas e normalizadas de Clostridium stricto sensu e negativamente associados às de Staphylococcus.
QUAIS SÃO AS CONSEQUÊNCIAS PRÁTICAS?
Este estudo mostra que é importante compreender o impacto dos diferentes nutrientes utilizados na microbiota intestinal dos recém-nascidos TFPN, de modo a ter um efeito benéfico na sua saúde a curto e longo prazo.