Uma análise do micobioma em diferentes cancros revela o envolvimento de fungos em tumores gastrointestinais e pulmonares
ARTIGO COMENTADO - Fase adulta
Pelo Prof. Harry Sokol
Gastroenterologia e Nutrição, Hospital Saint-Antoine, Paris, França
Comentário ao artigo original de Anders B. Dohlman et al. Cell 2022 [1]
Os microrganismos fúngicos (micobiota) são um componente numericamente pequeno do microbiota humano, embora seja altamente imunorreativo. Pouco se sabe sobre o papel da micobiota nos cancros humanos. A análise de cancros de diferentes órgãos e locais do corpo revelou a presença de uma micobiota associada a tumores, a uma taxa de uma célula fúngica por cada 10.000 células tumorais. No cancro do pulmão, o Blastomyces estava associado ao tecido tumoral. Nos cancros gástricos, níveis elevados de Candida estavam associados à expressão de vias imunitárias pró-inflamatórias, enquanto nos cancros do cólon, Candida era preditiva de doença metastática e atenuava a adesão celular. Em vários locais gastrointestinais, várias espécies de Candida foram enriquecidas em amostras de tumores e a presença de ADN de Candida associado ao tumor foi preditiva de uma diminuição da sobrevivência. A presença de Candida em tumores gastrointestinais humanos foi confirmada por sequenciação ITS de amostras de tumores e por uma abordagem de cultura numa coorte independente. Estes dados envolvem a micobiota na patogénese dos cancros gastrointestinais e sugerem que o ADN fúngico associado ao tumor pode servir como biomarcador de diagnóstico ou prognóstico.
O que é que já sabemos sobre isto?
O cancro é uma das principais causas de morte em todo o mundo. A sua tumorigénese, progressão e resposta ao tratamento são influenciadas por várias interações entre o sistema imunitário do hospedeiro e as bactérias da microbiota. No entanto, o papel dos fungos (micobiota) nestes processos permanece largamente inexplorado. Os fungos e as bactérias cocolonizam o trato digestivo, o epitélio cutâneo, o trato respiratório e os órgãos reprodutivos dos mamíferos, formando um ecossistema complexo de interações micróbio-micróbio e hospedeiro-micróbio com implicações importantes para a saúde humana. Embora as infeções fúngicas sejam responsáveis por mais de 1,5 milhões de mortes por ano em todo o mundo, representam apenas 0,1% do ADN microbiano presente no intestino, o que sugere uma influência desproporcionada das espécies deste reino no microbioma global e na imunidade do hospedeiro. Quer se trate de vírus, bactérias ou fungos, acumulam-se provas científicas da existência de uma ligação entre o microbioma humano, o cancro e as suas consequências. Nos últimos anos, foram observados vários casos de associação entre espécies bacterianas e o desenvolvimento/progressão do cancro. O Helicobacter pylori é responsável por cerca de 75% do risco atribuível ao cancro gástrico, enquanto a Escherichia coli genotóxica, o Bacteroides fragilis, o Streptococcus bovis/gallolyticus e o Fusobacterium nucleatum foram implicados na carcinogénese colorretal [2]. O que estas bactérias têm em comum é a sua capacidade de causar inflamação crónica, características que se pensa contribuírem para o seu potencial tumorigénico. Relatórios recentes identificaram também bactérias intracelulares em muitos tipos de tumores [3].
O micobioma desempenha um papel fundamental na ativação da imunidade inata no intestino. As toxinas fúngicas e as aminas bioativas têm sido associadas à carcinogénese. Estudos experimentais recentes apoiam o envolvimento de fungos no cancro em determinados contextos [4]. Os dados de sequenciação de bancos de tumores mostram a presença de sequências microbianas, mas a componente fúngica continua por explorar.
Quais são as principais conclusões deste estudo?
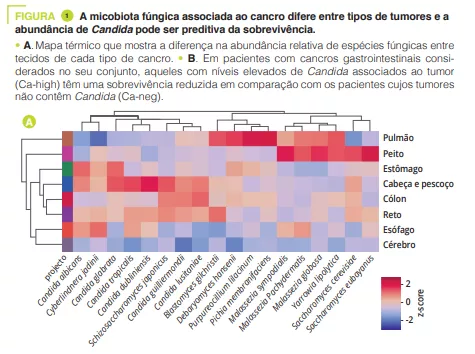
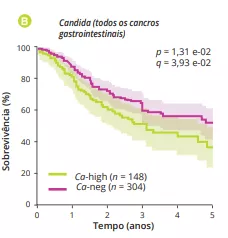
Ao analisar vários tipos de cancro utilizando o “The Cancer Genome Atlas“ (TCGA), os autores extraíram perfis do micobioma associado ao tumor com uma resolução ao nível das espécies. Depois de eliminar a contaminação e os sinais falsos positivos, os autores verificaram que as composições fúngicas variavam de acordo com o tipo de cancro, sendo alguns fungos específicos do tipo de tumor, tanto para locais gastrointestinais como não gastrointestinais (Figura 1A). No geral, foi encontrada até uma célula fúngica por cada 10 000 células tumorais humanas, uma taxa consistente com o facto de os fungos representarem 0,1-1% do microbioma e de se estimar que as bactérias representem pouco menos de 1% das células encontradas nos tumores [2, 3]. Verificou-se que várias espécies de Candida, Saccharomyces cerevisiae e Cyberlindnera jadinii eram muito abundantes nos tumores gastrointestinais, enquanto as espécies de Blastomyces e Malassezia eram abundantes nos tumores do pulmão e da mama, respetivamente. Os autores demonstraram depois que várias espécies de Candida estão vivas e transcritivamente ativas no tumor. Por fim, a abundância de certos fungos no tumor poderia prever a expressão genética do tumor hospedeiro, o estado da doença e a sobrevivência (Figura 1B), embora este facto esteja ainda por confirmar. Em conjunto, estes resultados implicam os fungos, e Candida em particular, na patogénese dos cancros gastrointestinais, mas também sugerem o seu potencial como alvo terapêutico e ferramenta de prognóstico.
Pontos chave
- Uma análise do micobioma em diferentes cancros mostra a presença de fungos no tecido tumoral
- Os tumores gastrointestinais contêm Candida viva e transcritivamente activa
- O ADN da Candida é abundante em certos tecidos tumorais, que podem ter um mau prognóstico
Quais são as consequências práticas?
Para além das bactérias, este estudo demonstra a presença de fungos em numerosos tumores digestivos e extradigestivos, com uma forma de especificidade de um tipo de tumor para outro e um potencial carácter preditivo de gravidade. Estes resultados sugerem um papel dos fungos no processo carcinológico e na sua gravidade. Poderão também abrir caminho para o desenvolvimento de novos biomarcadores ou de novos tratamentos contra o cancro que visem o componente fúngico.
CONCLUSÃO
Uma análise de múltiplos cancros digestivos e extradigestivos identificou fungos associados a tumores e, em particular, um enriquecimento em Candida nos cancros gastrointestinais. Os fungos poderiam desempenhar um papel na carcinogénese. O ADN fúngico associado ao tumor poderia servir de marcador de prognóstico neste contexto e os fungos poderiam constituir um novo alvo terapêutico em oncologia.

"Interesting developments. Thank you for caring about humanity." -sturehp (From Biocodex Microbiota Institute on X)
"Tumour-associated fungal DNA may serve as diagnostic or prognostic biomarkers. Very interesting. I am curious to see what comes out of this." -Just me. (From Biocodex Microbiota Institute on X)
1. Dohlman AB, Klug J, Mesko M, et al. A pan-cancer mycobiome analysis reveals fungal involvement in gastrointestinal and lung tumors. Cell 2022 ; 185 : 3807-22.e12.
2. Sepich-Poore GD, Zitvogel L, Straussman R, et al. The microbiome and human cancer. Science 2021 ; 371 : eabc4552.
3. Nejman D, Livyatan I, Fuks G, et al. The human tumor microbiome is composed of tumor type-specific intracellular bacteria. Science 2020 ; 368 : 973-80.
4. Alam A, Levanduski E, Denz P, et al. Fungal mycobiome drives IL-33 secretion and type 2 immunity in pancreatic cancer. Cancer Cell 2022 ; 40 : 153-67.e11.