O que é que já sabemos sobre isto?
Verifica-se um claro aumento da prevalência de doenças alérgicas. Foi demonstrado que as crianças que vivem no campo são menos suscetíveis de sofrer de asma do que as que vivem nas cidades. Em casa, o pó é a principal fonte de bactérias e fungos; a sua composição reflete o ambiente interior, influenciado pelas atividades exteriores (agricultura), materiais de construção e animais.
O desenvolvimento da microbiota intestinal durante os primeiros 1000 dias de vida tem um impacto no desenvolvimento subsequente de patologias alérgicas. Certos fatores bem conhecidos influenciam a composição da microbiota intestinal de um bebé: antibióticos, modo de parto e dieta. Pensa-se que a disbiose resultante favorece o desenvolvimento subsequente de doenças alérgicas. Em contrapartida, o aleitamento materno e o parto vaginal protegem contra o desenvolvimento subsequente de doenças alérgicas; a microbiota intestinal destes bebés caracteriza-se por uma predominância de bifidobactérias, nomeadamente Bifidobacterium breve. O contacto reduzido com a natureza promove a disbiose intestinal, com desregulação do equilíbrio imunitário Th1/Th2 a favor de Th2, que é a resposta imunitária adaptativa envolvida nas doenças alérgicas (Cukrowska Nutrients).
Os mecanismos pelos quais a disbiose intestinal no início da vida está envolvida no desenvolvimento de alergias e asma são pouco conhecidos. O pó das quintas e os lipopolissacáridos bacterianos induzem tolerância às endotoxinas, reduzindo assim a asma alérgica.
Quais são as principais conclusões deste estudo?
Os autores compararam as exposições ambientais urbanas e rurais na China num estudo com humanos e ratos. A coorte humana EuroPrevall-INCO incluiu 5.139 crianças urbanas e 5.542 crianças rurais em idade escolar. A prevalência de alergias alimentares e especialmente de asma, rinite e eczema aumentou nas crianças urbanas (p<0,001).
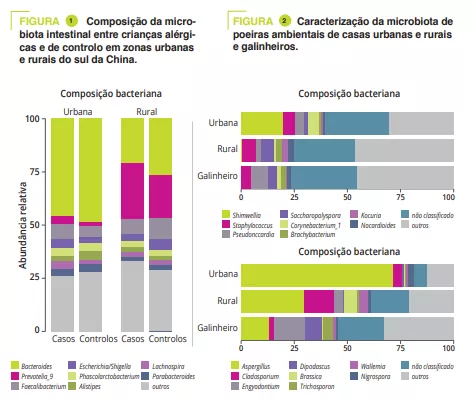
Um estudo caso-controlo incluiu 225 crianças: 151 que viviam em cidades e 74 em zonas rurais. A microbiota intestinal de todas as crianças foi analisada por sequenciação do gene rRNA 16S e as vias metabólicas foram avaliadas por shotgun. Foram recolhidos dados clínicos e testes alérgicos. O rácio Prevotella/Bacteroides foi significativamente mais elevado nas crianças rurais (p < 0,001); esta diferença deveu-se à Prevotella_9, que representou cerca de 25% das variantes amplificadas nas crianças rurais e < 5% nas crianças urbanas (Figura 1). No entanto, não houve diferença na composição da microbiota intestinal entre casos e controlos, quer na população rural quer na urbana. A análise das vias metabólicas revelou 14 vias diferentes entre urbano/rural e 9 entre casos/ controlos. Entre estas, a via que produz L-lactato foi fortemente associada à alergia, e a via de degradação do açúcar e a via de síntese de lipopolissacarídos estavam mais fortemente presentes na microbiota das crianças do grupo de controlo.
Para simular a exposição a ambientes microbianos, foram recolhidas amostras de pó de colchão de 10 famílias rurais e 10 famílias urbanas, bem como de 5 galinheiros de famílias rurais (que poderiam fazer parte do ambiente microbiano nas casas das famílias rurais). Enterobacteriaceae e Rhizobiaceae predominaram apenas nas poeiras de residências urbanas (Figura 2). A diversidade a e a quantidade de endotoxinas são maiores nas poeiras das casas rurais do que nas casas urbanas e nos galinheiros. Por último, a proporção de bactérias potencialmente patogénicas foi significativamente mais elevada nas poeiras das habitações urbanas. Além disso, Aspergillaceae predominou nas poeiras das casas urbanas, enquanto Trichocomaceae (género Penicillium) foi mais abundante nas poeiras das casas rurais (onde a diversidade foi maior) e dos galinheiros (Figura 2).
Para testar o impacto do pó ambiental nas alergias respiratórias através da alteração da microbiota intestinal, os investigadores expuseram ratinhos ao pó por via intranasal (modelo de alergia induzido pela ovalbumina). A exposição prévia ao pó das casas em zonas rurais atenuou a inflamação alérgica (infiltração de eosinófilos nas vias respiratórias e presentes na lavagem broncoalveolar (LBA), aumento da IgE sérica específica). O aumento de bactérias potencialmente patogénicas foi menor no grupo de ratos expostos a poeiras rurais; a abundância intestinal de Bacteroidales aumentou e a de Clostroidales (incluindo espécies pertencentes às famílias Lachnospiraceae e Ruminococcaceae) diminuiu em ratos de controlo expostos a PBS, bem como nos expostos a poeiras urbanas. Finalmente, a abundância relativa de Bacteroides e Ruminiclostridium na microbiota intestinal correlacionou-se com os eosinófilos presentes no LBA (r = 0,59 e p = 0,001 e r = -0,45 e p = 0,05, respetivamente).
Quais são as consequências práticas
A modulação precoce da microbiota intestinal, visando o efeito benéfico da microbiota em poeiras das casas rurais, poderia ajudar a prevenir o desenvolvimento de patologias alérgicas.

 Disbiose da microbiota intestinal e autismo: desvendado o papel da alimentação
Disbiose da microbiota intestinal e autismo: desvendado o papel da alimentação
 Autismo: um novo protocolo de transplante de microbiota fecal apresenta resultados promissores
Autismo: um novo protocolo de transplante de microbiota fecal apresenta resultados promissores