Badania coraz częściej wskazują na istnienie odrębnych sygnatur mikrobiologicznych odpowiadających za rozmaite alergie pokarmowe. Potwierdzają one, że mikrobiota odgrywa kluczową rolę w rozwoju alergii. Wyniki badań wieloletnich opublikowane niedawno w czasopiśmie „Journal Of Allergy & Clinical Immunology” rzucają nowe światło na możliwe powiązania między rozwojem alergii na orzeszki ziemne a stanem mikrobioty.
Mając na uwadze rozwój alergii we wczesnym dzieciństwie, naukowcy zbadali mikrobiotę dzieci obciążonych ryzykiem rozwoju alergii na orzeszki ziemne w wieku 10 miesięcy (SD: 3,1), a następnie w wieku 9 lat (SD: 0,6). Stwierdzono, że u 35 (28,7%) dzieci w tej grupie rozwinęła się alergia na orzeszki ziemne przed ukończeniem 9. roku życia.
Odmienna sygnatura mikrobioty jelitowej od pierwszych miesięcy życia
Grupa PA (osoby uczulone na orzeszki ziemne) składająca się z 35 dzieci wykazywała mniej zróżnicowaną mikrobiotę w momencie włączenia do badania (p = 0,014) niż grupa NPA (osoby nieuczulone na orzeszki ziemne). Mikrobiota ta ulega zróżnicowaniu wraz z wiekiem, podczas gdy mikrobiota grupy NPA pozostaje stabilna.
Po osiągnięciu wieku 9 lat obie grupy cechowały się porównywalną różnorodnością mikrobioty.
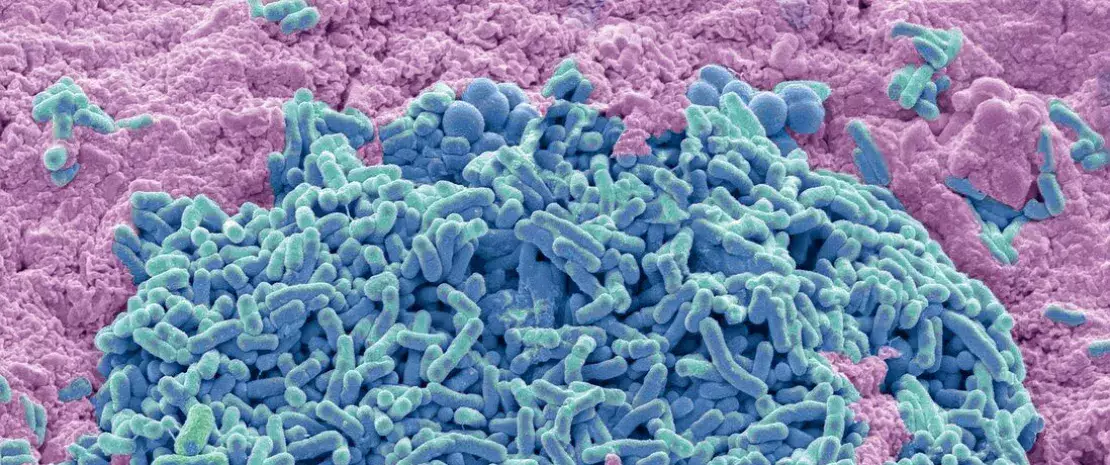
W momencie włączenia do badania grupa PA charakteryzowała się wyższym poziomem liczebności bakterii Clostridium sensu stricto 1 sp, podczas gdy bakterie Streptococcus sp występowały częściej w grupie NPA. U dzieci w wieku 9 lat względna liczebność tych dwóch gatunków unormowała się w obu badanych grupach. Z kolei liczebność gatunków Bifidobacterium sp spadła w grupie PA i zwiększyła się w grupie NPA.
Stwierdzono, że rozwój alergii jest związany ze zmianą poziomów 139 metabolitów metabolomu (FDR ≤ 0,05).
Te metabolity są z kolei powiązane ze szlakiem metabolizmu histydyny (FDR = 0,037, wpływ szlaku = 0,28).
Przebadano w szczególności sześć krótkołańcuchowych kwasów tłuszczowych. W grupie PA odnotowano spadek poziomu maślanu i izowalerianu, podczas gdy poziom izowalerianu pozostał na niezmienionym poziomie w grupie NPA przy jednoczesnym wzroście maślanu.
Czy istnieje patofizjologiczny mechanizm alergii na orzeszki ziemne?
Autorzy badań wysunęli hipotezę, że mniejsza różnorodność mikrobioty u niemowląt z grupy PA może oznaczać, że ich jelita odznaczały się mniejszą stabilnością na etapie szybkiego rozwoju układu odpornościowego.
Spadek względnej liczebności bakterii Bifidobacterium sp, która znana jest z zastosowania jako probiotyk antyalergiczny i wywołuje apoptozę komórek tucznych u myszy, może również odgrywać rolę w rozwoju alergii.
Autorzy badania podkreślają również, że mikroorganizmy występujące w jelitach dzieci podatnych na rozwój tej alergii zawierają gatunki zdolne do wytwarzania metabolitów ze szlaku metabolicznego histydyny, prekursora histaminy, będącej charakterystycznym efektorem reakcji alergicznych.
 Mikroplastik w daniach na wynos = zagrożona flora jelit i jamy ustnej
Mikroplastik w daniach na wynos = zagrożona flora jelit i jamy ustnej
 Wszystko, co musisz wiedzieć o osi mikrobiota-jelita-mózg
Wszystko, co musisz wiedzieć o osi mikrobiota-jelita-mózg