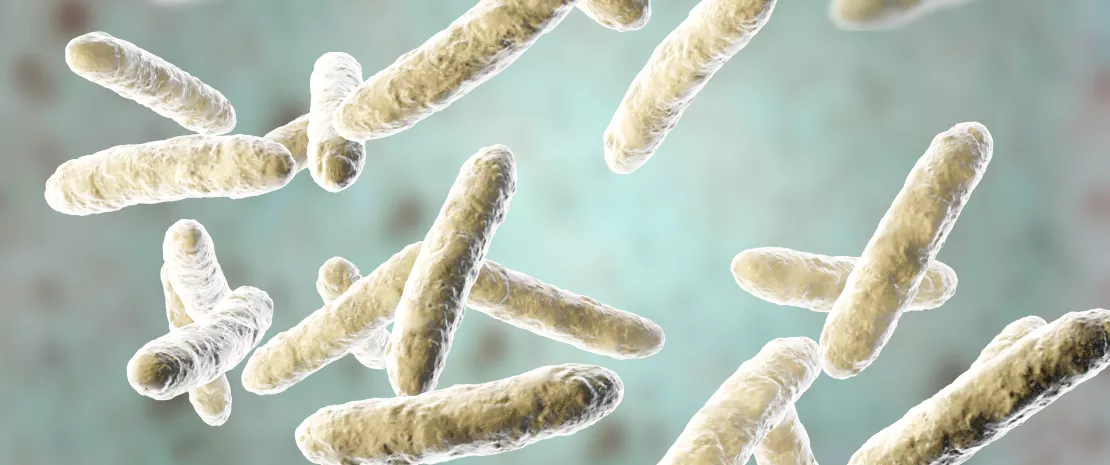
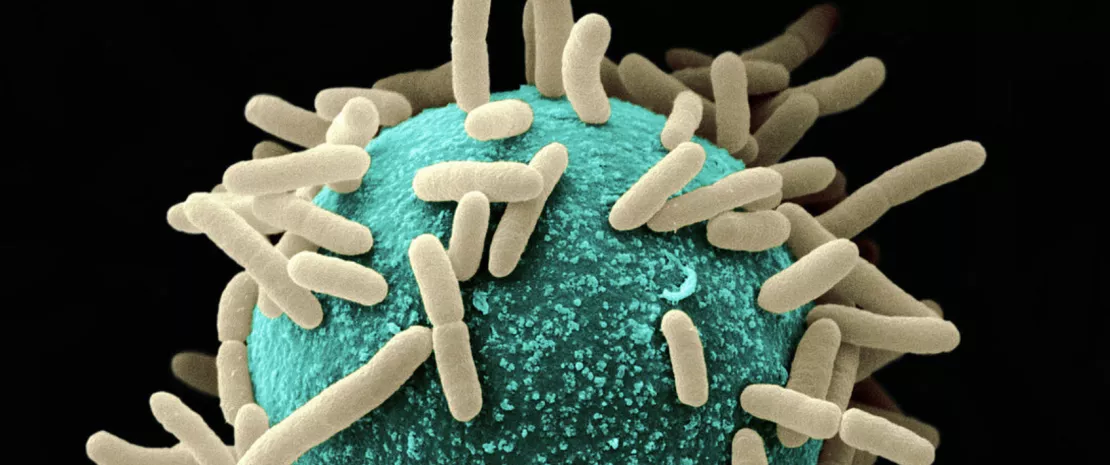
Um número crescente de estudos avança com a hipótese da existência de assinaturas microbiotas distintas de acordo com as alergias alimentares. Este campo de investigação contribui para um posicionamento da microbiota como um elemento fundamental no desenvolvimento destas alergias. Um novo estudo longitudinal publicado recentemente no Journal Of Allergy & Clinical Immunology fornece novos dados relativos às ligações que poderão existir entre o desenvolvimento de uma alergia a amendoins e a microbiota.
Esta alergia desenvolve-se geralmente durante a primeira infância e os investigadores estudaram a microbiota de crianças suscetíveis de manifestar um alergia aos amendoins aos 10 meses (SD: 3,1) e depois aos 9 anos (SD: 0,6). Dentro desta população, 35 (28,7%) crianças desenvolveram uma alergia ao amendoim antes dos 9 anos.
Uma assinatura da microbiota intestinal diferente desde os primeiros meses
Estas 35 crianças do grupo PA (Peanuts Allergy - Alergia a amendoins) apresentaram uma microbiota menos diversa inicialmente (p=0,014) do que o grupo NPA (Non Peanuts Allergy - Sem alergia a amendoins). Esta microbiota diversifica-se com a idade, ao passo que a do grupo NPA se mantém estável.
Aos 9 anos, os dois grupos apresentam uma diversidade microbiota comparável.
No início, o grupo PA apresenta uma maior proporção de Clostridium sensu stricto 1 sp, enquanto a Streptococcus sp é mais predominante no grupo NPA. Aos 9 anos, a abundância relativa destas duas espécies está normalizada nas duas populações. Em contrapartida, a espécie Bifidobacterium sp tem um declínio no grupo PA até se tornar mais presente na população NPA.
O desenvolvimento da alergia foi identificado como estando associado a uma modificação dos níveis de 139 metabolitos do metaboloma (FDR≤ 0,05).
Estes metabolitos estão associados a uma via de metabolização da histidina (FDR = 0,037, impacto do percurso = 0,28).
Foram estudados especificamente seis ácidos gordos de cadeia curta. O grupo PA demonstra uma redução dos níveis de butirato e isovalerato enquanto o nível de isovalerato permanece estável no grupo NPA com um aumento do butirato.
E em comparação com um mecanismo fisiopatológico de alergia aos amendoins?
Os autores colocam a hipótese de que a diversidade inferior da microbiota dos bebés PA pode sugerir que estes possuem comunidades intestinais menos estáveis durante esta fase de desenvolvimento rápido do sistema imunitário.
A diminuição da abundância relativa da Bifidobacterium sp, conhecida pela sua utilização na probiótica antialérgica e por causar a apoptose dos mastócitos em ratos, pode igualmente desempenhar um papel no desenvolvimento das alergias.
Os autores destacam igualmente que os microrganismos presentes nos intestinos das crianças predispostas a desenvolver esta alergia, albergam espécies capazes de produzir metabolitos provenientes da via metabólica da histidina, precursora da histamina, efetora característica das reações alérgicas.

 Microbiota, chave para o diagnóstico precoce da doença de Alzheimer?
Microbiota, chave para o diagnóstico precoce da doença de Alzheimer?
 Será a microbiota intestinal, o novo segredo de juventude?
Será a microbiota intestinal, o novo segredo de juventude?