Microbiota intestinal, sistema nervioso central y desarrollo neurológico
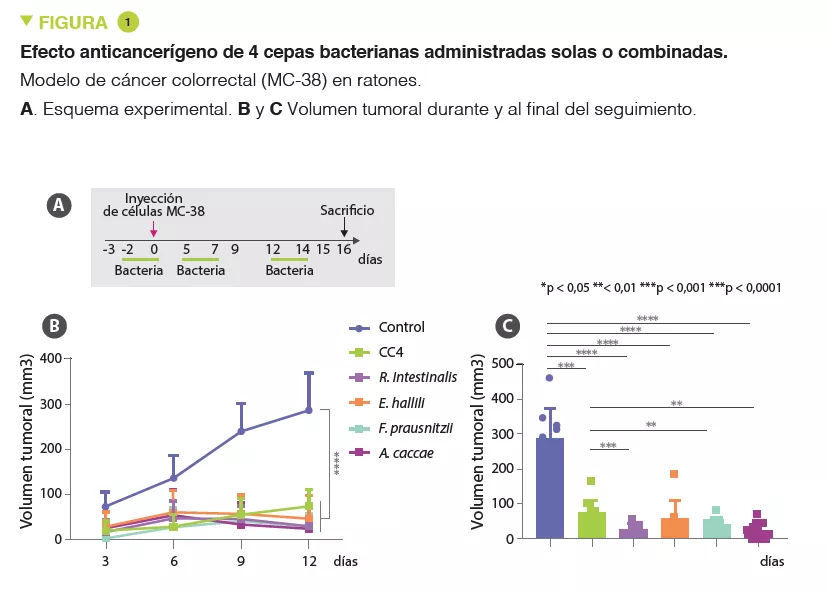
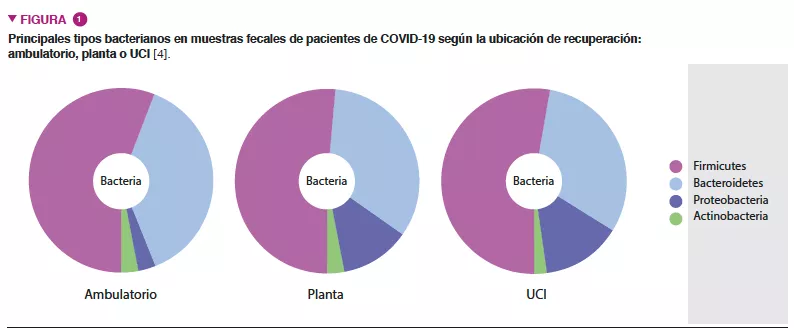
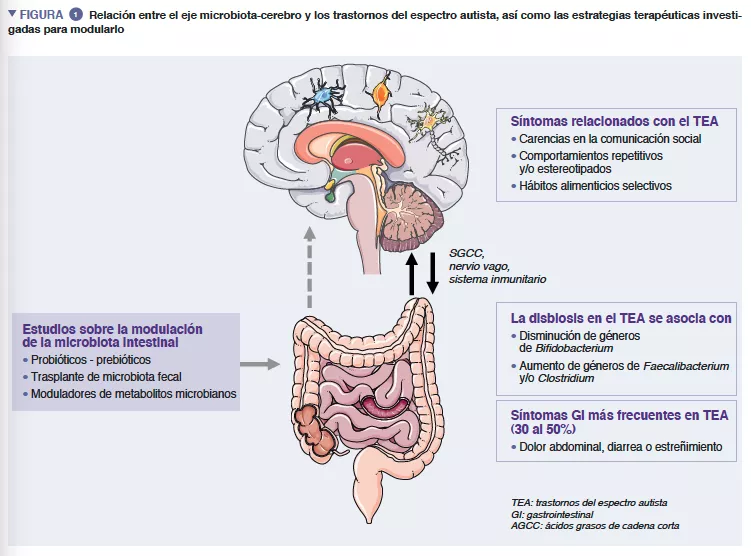
La microbiota intestinal humana (MI) está formada por aproximadamente 1013 microorganismos, principalmente bacterias, hongos y virus. La MI desempeña una función primordial en la salud humana, garantizando la función barrera del intestino, la modulación de la respuesta inmunitaria y la síntesis metabólica, pero también una protección directa frente a infecciones. La disbiosis caracterizada por una MI desequilibrada se ha asociado con numerosas patologías como las enfermedades inflamatorias del intestino, tumores, diabetes u obesidad [4]. Varios hallazgos fiables indican además importantes interacciones entre la MI y el sistema nervioso central (SNC) [5] (Figura 1).
Los metabolitos microbianos (principalmente los ácidos grasos de cadena corta) y los moduladores inmunitarios son los mediadores de la interacción recíproca entre el cerebro y la MI, atravesando directamente las barreras hematoencefálica y sanguínea, e indirectamente, mediante la estimulación del nervio vago [6]. Las pruebas respaldan la implicación de la MI en la regulación tanto del comportamiento humano como de las funciones intelectuales —en concreto, de las habilidades sociocomunicativas— aunque el mecanismo exacto aún se desconoce [5].
Los TEA son trastornos del desarrollo neurológico caracterizados por alteraciones en la comunicación social, en las interacciones sociales, por comportamientos repetitivos o estereotipados, que se inician en la infancia y afectan aproximadamente a 1% de la población general. El determinismo del TEA se debe principalmente a factores genéticos, con una heredabilidad estimada que llega al 0,8-0,9, pero las circunstancias ambientales prenatales y postnatales pueden actuar como factores precipitantes o moduladores de la gravedad de los síntomas. La etapa del desarrollo del cerebro en un momento temprano de la vida se solapa con la de la MI. Esta empieza a desarrollarse poco después del nacimiento, y su composición se estabiliza en un perfil similar al de un adulto en torno a los 3 años. En la composición temprana de la MI influyen en gran medida factores ambientales tales como el lugar de nacimiento, el modo de parto, la lactancia materna y los xenobióticos (por ejemplo, la administración de antibióticos).
Los ratones axénicos son un modelo que carece de cualquier tipo de microorganismo, es decir, son microbiológicamente axénicos (no se pueden cultivar microorganismos que provengan de ratones axénicos). Los modelos murinos axénicos son valiosos para descifrar los mecanismos subyacentes de las funciones de la MI en el desarrollo neurológico, pero también en la relación entre microbioma y enfermedad. Varios estudios demostraron que los ratones axénicos presentan (i) un defecto en la permeabilidad de la barrera hematoencefálica; (ii) un mayor volumen cerebral; (iii) una mayor expresión genética de la microglía inmadura y una menor capacidad de respuesta inmunitaria de la microglía; (iv) un aumento de la mielinización; y (v) una disminución de la expresión del factor neurotrófico derivado del cerebro y en una subunidad de los receptores de N-metil-D-aspartato [5, 7] Todos estos datos destacan la función de la MI en la formación y la integridad de la barrera hematoencefálica, la neurogénesis, la homeostasis de la microglía, la mielinización y el crecimiento y la función del cerebro.
Microbiota intestinal, síntomas gastrointestinales y trastornos del espectro autista
Los ratones axénicos mostraron comportamientos de tipo autista, como evitación social, comportamientos repetitivos o estereotipados, falta de interés en la actualidad social. Algunos de estos comportamientos desaparecieron tras la colonización con una MI de ratones silvestres, mientras que la colonización con MI de modelos murinos con TEA aumentó dichos comportamientos. Efectivamente, parece que la MI es fundamental para la programación y presentación de las habilidades sociales y los comportamientos adaptativos [8].
Cada vez hay más pruebas que demuestran que los síntomas GI están sobrerrepresentados en los niños con TEA. Los síntomas GI como el dolor abdominal, el estreñimiento y la diarrea, aparecen en casi el 30-50% de los pacientes con TEA y afectan en gran medida en la calidad de vida de los niños [1]. La gravedad de los síntomas gastrointestinales se correlacionó con la gravedad de los síntomas autistas, y la disbiosis intestinal está ampliamente documentada, incluso aunque aún no exista una firma microbiana específica relacionada con los síntomas autistas. Los estudios que exploran la MI han descrito diferencias en la diversidad de la microbiota, así como patrones anormales de metabolitos, en comparación con pacientes de control sanos. Dos metanálisis recientes que exploraron la composición de la MI en pacientes con TEA observaron un descenso de los géneros Bifidobacterium y un aumento de Faecalibacterium y Clostridium en pacientes con TEA [9, 10] en comparación con los controles sanos. La exploración del metaboloma fecal también demostró un aumento de p-cresol, un metabolito bacteriano derivado de la tirosina, en personas con TEA. En su conjunto, todos estos datos pueden indicar una posible asociación entre las anomalías de la MI y los síntomas GI en pacientes con TEA.
Sin embargo, la mayoría de los estudios tienen resultados heterogéneos y limitaciones metodológicas. Factores de confusión como son distintos países con distintos estilos de vida y hábitos alimenticios son los mayores inconvenientes de estos estudios. De hecho, un estudio reciente de una gran muestra de 247 personas con TEA no describió vínculos directos entre el diagnóstico del TEA o síntomas autistas y la disbiosis de la MI. La disbiosis se asociaba a una alimentación menos diversificada, un factor común de los pacientes con TEA [8].
Modulación de la microbiota intestinal en los trastornos del espectro autista
Un número cada vez mayor de estudios ha explorado la posible repercusión de estrategias terapéuticas basadas en la microbiota para mejorar los síntomas GI y los síntomas principales en personas con TEA.
En el TEA se han utilizado probióticos (microorganismos vivos) que podrían tener un efecto beneficioso en pacientes con este trastorno. Algunos estudios preclínicos han notificado un aumento de las interacciones sociales tras una suplementación con probióticos (Bacteroides fragilis NCTC9343, Lactobacillus reuteri MM4-1A) en modelos murinos con TEA. La mejora de la comunicación social se relacionó con una mayor expresión de oxitocina en el SNC. En humanos, numerosos estudios han descrito efectos positivos de los tratamientos con probióticos en la composición de la MI y en los síntomas GI en el TEA [11]. Sin embargo, pocos han notificado una mejoría de los síntomas autistas principales. En la mayoría de los ensayos clínicos que suministraron probióticos a personas con autismo se observó una falta de uniformidad en cuanto a los probióticos, a la posología diaria o total, y la duración de todo el tratamiento. Aunque algunos estudios sugieren que los probióticos podrían ser interesantes para prevenir los síntomas GI en pacientes con TEA, es necesario replicar los resultados para garantizar el efecto positivo de dicha estrategia. De la misma manera, se ha explorado la eficacia de los prebióticos, como el galactoligosacárido (GOS) o el fructoligosacárido en el TEA [12]. Se observó una alteración de la MI y una disminución del interés social en ratones con estrés crónico. Utilizando este modelo murino, se asoció la administración de prebióticos a un aumento de las interacciones sociales en estos ratones. En humanos, se ha observado que el consumo de GOS asociado a una alimentación sin caseína ni gluten, mejoraba los síntomas GI y las interacciones sociales, junto con un aumento de la abundancia de Bifidobacterium en la MI. Es necesario realizar estudios clínicos aleatorizados con doble ciego para confirmar estos hallazgos preliminares.
También se ha estudiado el trasplante de microbiota fecal (TMF) en el TEA. El TMF consiste en realizar un trasplante de MI de un donante para modificar la MI del receptor. Actualmente, su eficacia en la infección por Clostridioides difficile está suficientemente demostrada, incluso en niños. Un reciente ensayo clínico exploratorio no aleatorizado y sin doble ciego, en el que participaron 18 niños diagnosticados de TEA y con síntomas GI, evaluó el efecto de la terapia de transferencia de microbiota (TTM), un protocolo modificado del TMF [13]. La TTM consistía en un tratamiento de dos semanas con antibióticos, un lavado intestinal, antes de recibir el tratamiento con TTM que consistía en una dosis elevada por vía oral o rectal seguida de una dosis oral de mantenimiento durante 7 u 8 semanas. Se observaron acontecimientos adversos al comienzo del tratamiento con vancomicina (comportamientos perturbadores, hipercinesia), que desaparecieron espontáneamente tras 3 días de tratamiento. El protocolo de la TTM condujo a una mejoría significativa de los síntomas GI tras el consiguiente estudio de 8 semanas. De manera aún más sorprendente, también se observó una mejoría en los síntomas autistas principales (comportamientos estereotipados y repetitivos, habilidades de comunicación social) 8 semanas después de la TTM. Curiosamente, la mejoría de los síntomas GI y de los síntomas autistas perduró 2 años después del tratamiento y se relacionó con el aumento de la diversidad de la MI [14]. Dos años después de la TTM, la reducción media de la puntuación total de la escala de evaluación de síntomas gastrointestinales (GSRS) seguía siendo superior al 50%. Los cambios en los síntomas autistas medidos con la escala de evaluación del autismo infantil (CARS), la escala de sensibilidad social (SRS) o la lista de comprobación del comportamiento autista (ABC) se relacionaron positivamente con los cambios porcentuales en las puntuaciones de la GSRS. Estos resultados aún no se han confirmado con estudios aleatorizados con doble ciego y en comparación con placebo.
Recientemente, un ensayo clínico experimental abierto sobre el TEA ha explorado el efecto de un adsorbente oral con restricción GI (AB-2004) que modula varios metabolitos de la MI. Los autores describieron una disminución de los comportamientos ansiosos en ratones, impulsada por una disminución de los metabolitos de la microbiota intestinal [15]. El estudio presentó además los resultados de un ensayo clínico en el que se administró una dosis de AB-2004 ajustada al peso a 30 adolescentes con TEA durante 8 semanas. En la semana 8, se observaron niveles reducidos de metabolitos de MI en plasma y orina. Lo más interesante es que, después del tratamiento, hubo menos pacientes con síntomas gastrointestinales, pero también con menos comportamientos asociados al TEA, ansiedad e irritabilidad. Además, hubo un efecto remanente con una persistencia de la eficacia 4 semanas después de la interrupción del tratamiento [15]. Aún hay que determinar los factores que relacionan las mejorías clínicas y la administración de AB-2004, puesto que no se han estudiado ciertos factores indirectos, como el efecto de AB-2004 en cambios de la alimentación, el estado inmunitario o la función gastrointestinal. Es necesaria la realización de estudios más amplios, con doble ciego y comparativos con placebo, para seguir diseccionando el papel del AB-2004 en la comunicación social en humanos. En un contexto de falta de tratamiento específico para los síntomas GI y los síntomas autistas en pacientes con TEA, es necesario encontrar nuevas estrategias terapéuticas bien toleradas dirigidas a la MI o a los metabolitos microbianos, como el TMF/TTM, en particular en las etapas tempranas y críticas del desarrollo cerebral durante la infancia.mental abierto sobre el TEA ha explorado el efecto de un adsorbente oral con restricción GI (AB-2004) que modula varios metabolitos de la MI. Los autores describieron una disminución de los comportamientos ansiosos en ratones, impulsada por una disminución de los metabolitos de la microbiota intestinal [15]. El estudio presentó además los resultados de un ensayo clínico en el que se administró una dosis de AB-2004 ajustada al peso a 30 adolescentes con TEA durante 8 semanas. En la semana 8, se observaron niveles reducidos de metabolitos de MI en plasma y orina. Lo más interesante es que, después del tratamiento, hubo menos pacientes con síntomas gastrointestinales, pero también con menos comportamientos asociados al TEA, ansiedad e irritabilidad. Además, hubo un efecto remanente con una persistencia de la eficacia 4 semanas después de la interrupción del tratamiento [15]. Aún hay que determinar los factores que relacionan las mejorías clínicas y la administración de AB-2004, puesto que no se han estudiado ciertos factores indirectos, como el efecto de AB-2004 en cambios de la alimentación, el estado inmunitario o la función gastrointestinal. Es necesaria la realización de estudios más amplios, con doble ciego y comparativos con placebo, para seguir diseccionando el papel del AB-2004 en la comunicación social en humanos.
En un contexto de falta de tratamiento específico para los síntomas GI y los síntomas autistas en pacientes con TEA, es necesario encontrar nuevas estrategias terapéuticas bien toleradas dirigidas a la MI o a los metabolitos microbianos, como el TMF/TTM, en particular en las etapas tempranas y críticas del desarrollo cerebral durante la infancia.