Mam na imię Jennifer, mam 32 lata i jestem menedżerką produktu w branży modowej.
Czy mogłabyś opisać zespół jelita drażliwego?
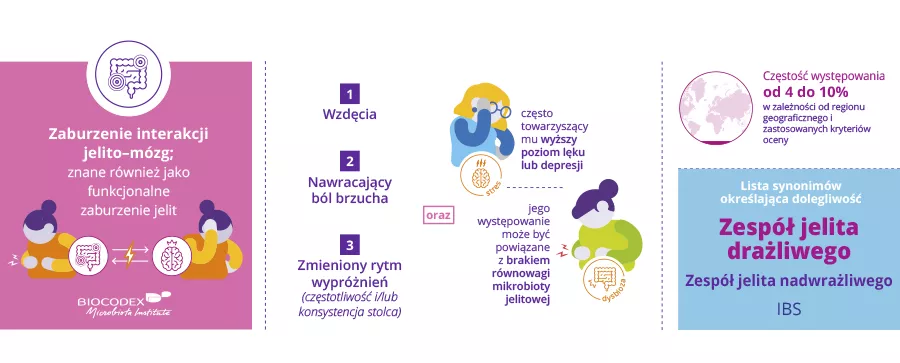
Zespół jelita drażliwego to przewlekła, niewidoczna i niezrozumiała choroba układu pokarmowego.
Jakie miałaś objawy?
Moimi pierwszymi objawami, co dziwne, były alergie pokarmowe, rozwinął się u mnie także zespół Raynauda: moje kończyny, dłonie i stopy są niezwykle zimne, bo krew przestaje w nich krążyć.
Miałam też bóle pleców, przez co musiałam nosić pas stabilizujący, gdy miałam 25 lat.
Jak długo trwała diagnoza?
Miałam te objawy przez 21 lat, a zostałam zdiagnozowana, mając 29 lat.
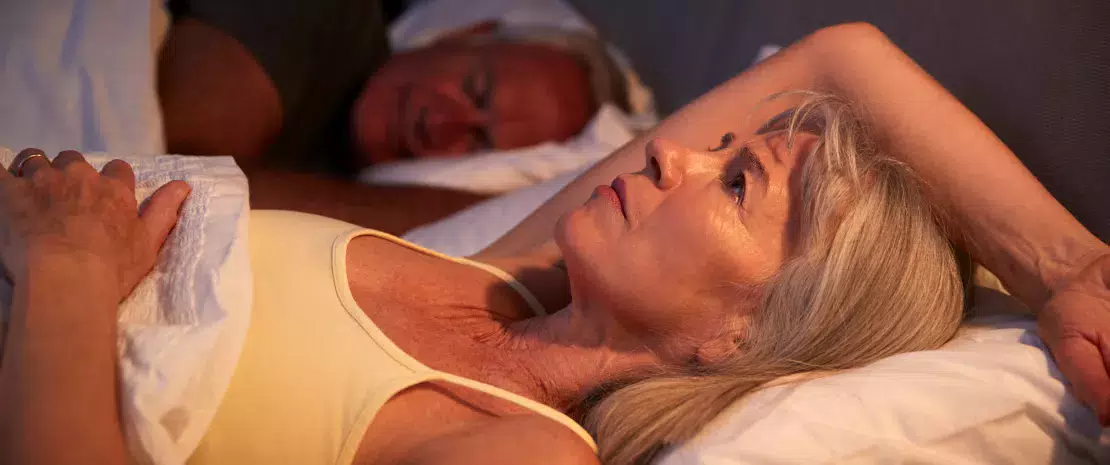
Jakie wydarzenie skłoniło Cię do szukania pomocy medycznej?
Pewnego ranka obudziłam się wyjątkowo zmęczona, byłam bardzo spóźniona do pracy. Wtedy się załamałam.
Gdzie szukałaś porady w związku ze swoimi objawami?
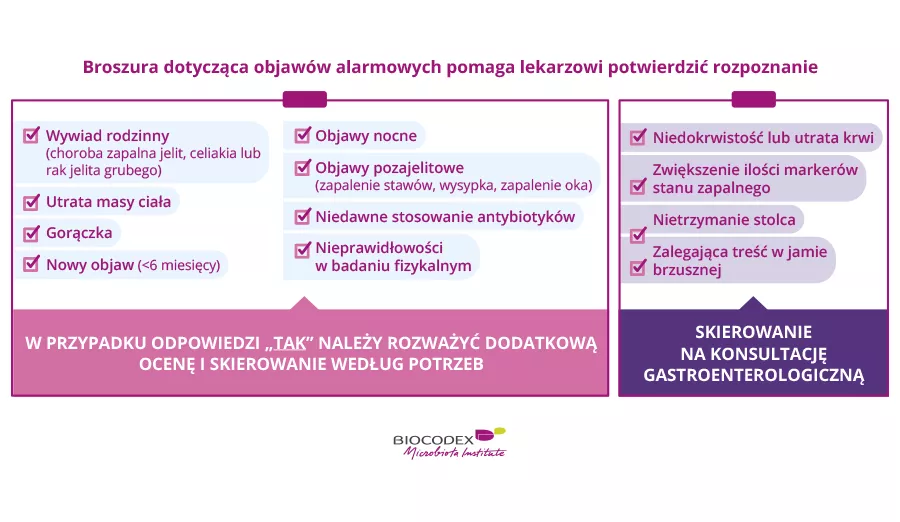
Początkowo szukałam porady u lekarzy ogólnych, u gastroenterologów, ale odpowiedzi były zawsze takie same: ponieważ początkowo miałam raczej zaparcia, podawano mi dużo środków przeczyszczających i nie drążono dalej tego tematu. Szukałam też porady u reumatologów i nigdy nie uzyskałam właściwej odpowiedzi, aż udałam się do pewnego gastroenterologa, który powiedział mi o tym zespole i diecie FODMAP.
Czym jest FODMAP?
To fermentujące cukry w żywności, które mogą być problemem dla osób z zespołem jelita drażliwego.
Czy wiesz, że Twoja mikrobiota jelitowa może odgrywać rolę w przypadku zespołu jelita drażliwego?
Wiedziałam, że moja mikrobiota przyczynia się do tego, od momentu, kiedy gastroenterolog uświadomił mi, że to moja dieta jest problemem. Gdy zmieniłam dietę, wdrożyłam protokół FODMAP i udało mi się ponownie zadbać o moją mikrobiotę, wszystkie objawy zniknęły. Ale tak zupełnie wszystkie.
Jak wygląda życie z zespołem jelita drażliwego na co dzień?
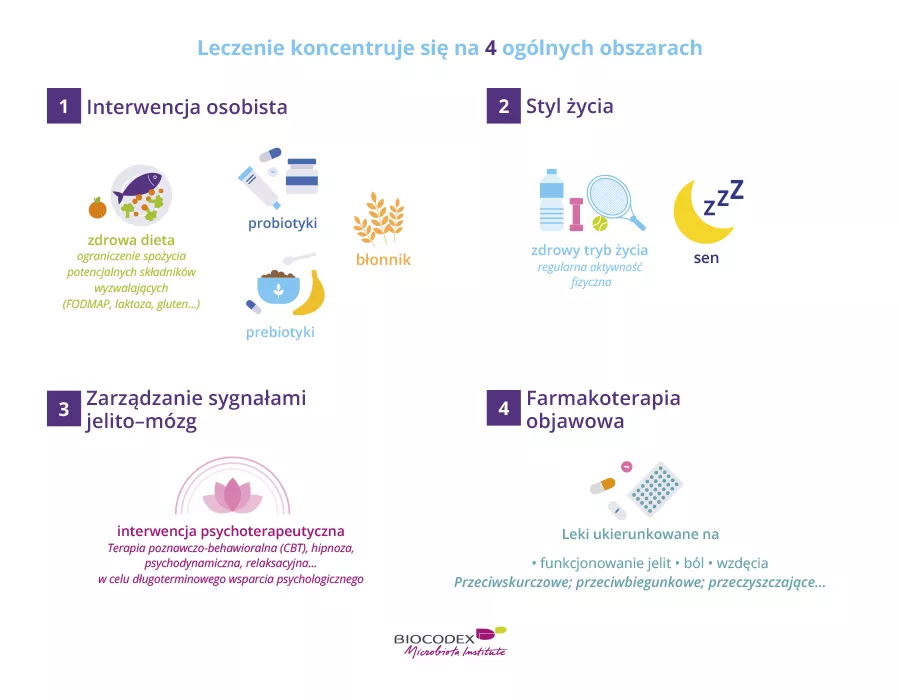
Na co dzień radzę sobie z chorobą, prowadząc zdrowy tryb życia. Muszę się dobrze wysypiać i uważać na to, co jem. Staram się też unikać wszelkich niepotrzebnych stresów, które mogłyby wpłynąć również na mój żołądek, a co za tym idzie, na głowę.
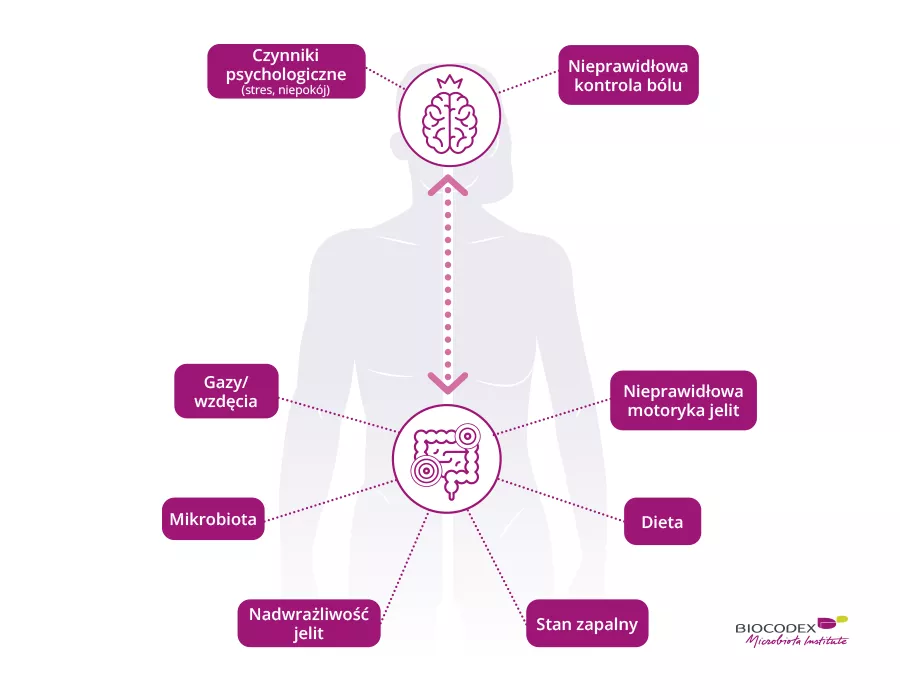
Co możesz powiedzieć o połączeniu jelit z mózgiem w odniesieniu do zespołu jelita drażliwego?
Dla mnie jelito drażliwe to dowód na to, że głowa i żołądek są całkowicie połączone. Dla mnie jelita to wręcz pierwszy mózg. Jak coś się psuje w żołądku, to z pewnością zacznie również psuć się w głowie.
Twoje przesłanie dla osób z zespołem jelita drażliwego?
Mam wiele porad dla takich osób i stworzyłam bloga foodmapers.com o tej tematyce, gdzie zebrałam wszystkie moje wskazówki.
Posłuchaj siebie, zaufaj sobie. Problem nie tkwi w Twojej głowie. Jeśli coś według Ciebie jest nie tak, może to być związane z Twoją mikrobiotą i sposobem trawienia.
Sama tego doświadczyłam. To nie może być tak, że przez 20 lat robi się prześwietlenia i badania ultrasonograficzne i ciągle słyszy się, że nic się nie dzieje. Oczywiście, że coś jest nie tak. Gdy już otrzyma się taką diagnozę, jest wiele rzeczy do zrobienia w kwestii odżywiania, niepokoju, stresu i snu.
Słowo na koniec
Myśl pozytywnie, ale przede wszystkim musisz nadal się badać, nie poddawać się i znaleźć pracowników służby zdrowia, którzy będą cię wspierać i pomogą ci odkryć przyczynę problemu.