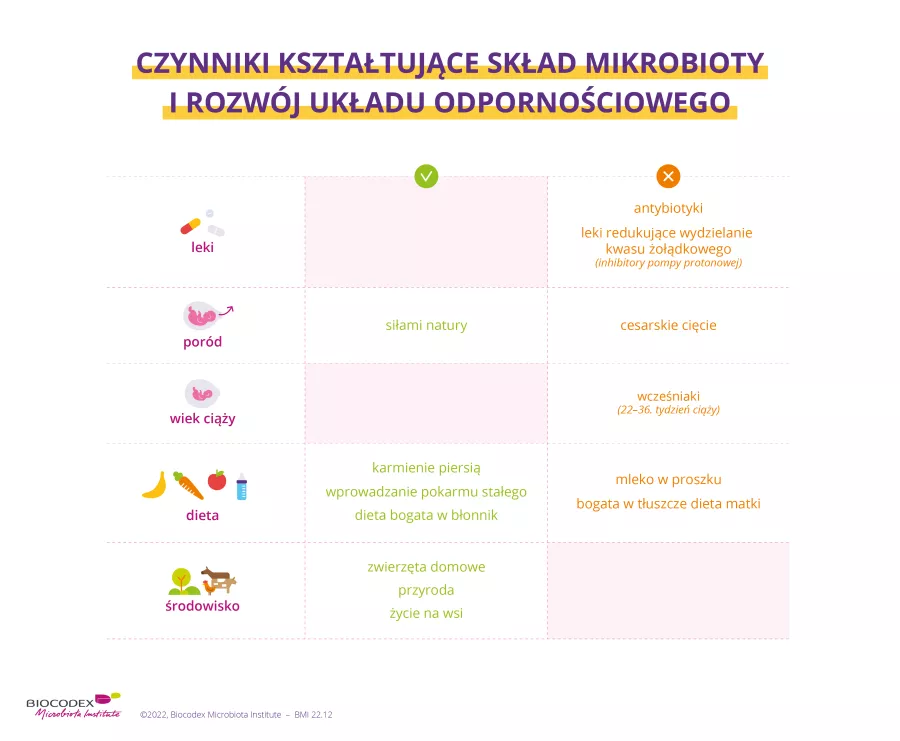
Oporność na antybiotyki: mikrobiota na pierwszym planie
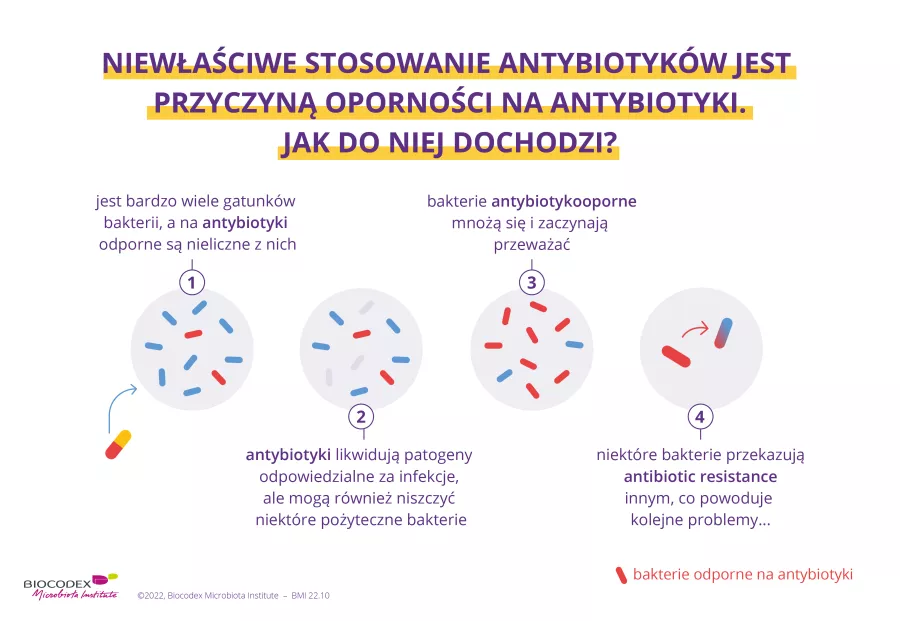
Masowe, często nieodpowiednie stosowanie antybiotyków powoduje, że są one coraz mniej skuteczne w leczeniu infekcji. Skutek jest taki, że wiele bakterii jest dziś na nie odpornych. W efekcie choroby zakaźne mogą być w 2050 r. jedną z najczęstszych przyczyn zgonów na świecie. Analiza światowego problemu zdrowotnego i jego wpływu na mikrobiotę.

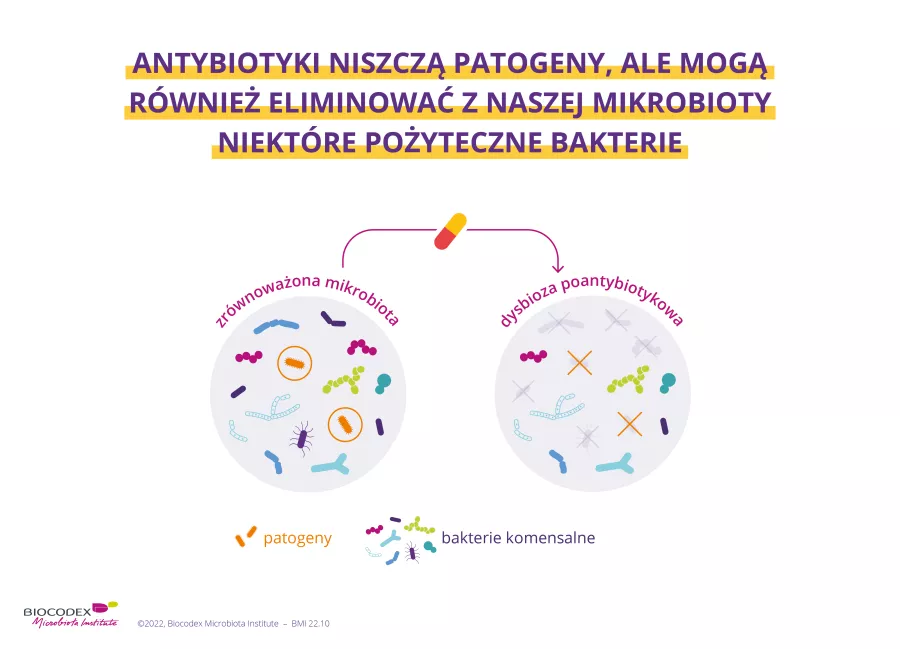
 Podwójne oblicze antybiotyków: Ratują życie i zaburzają mikrobiotę
Podwójne oblicze antybiotyków: Ratują życie i zaburzają mikrobiotę
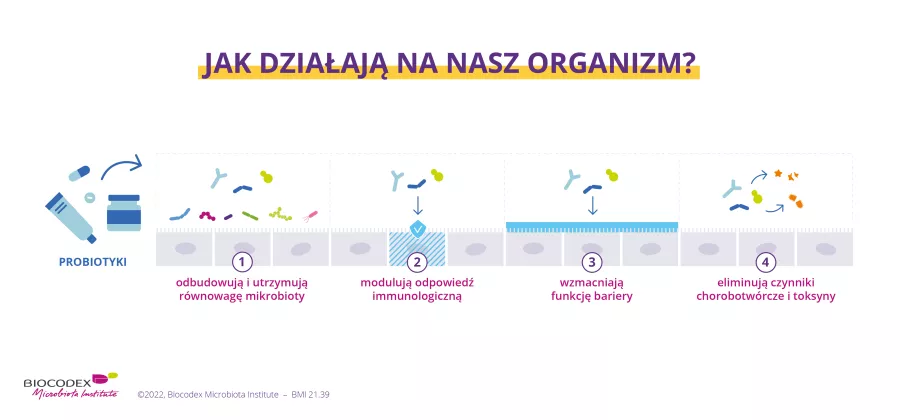
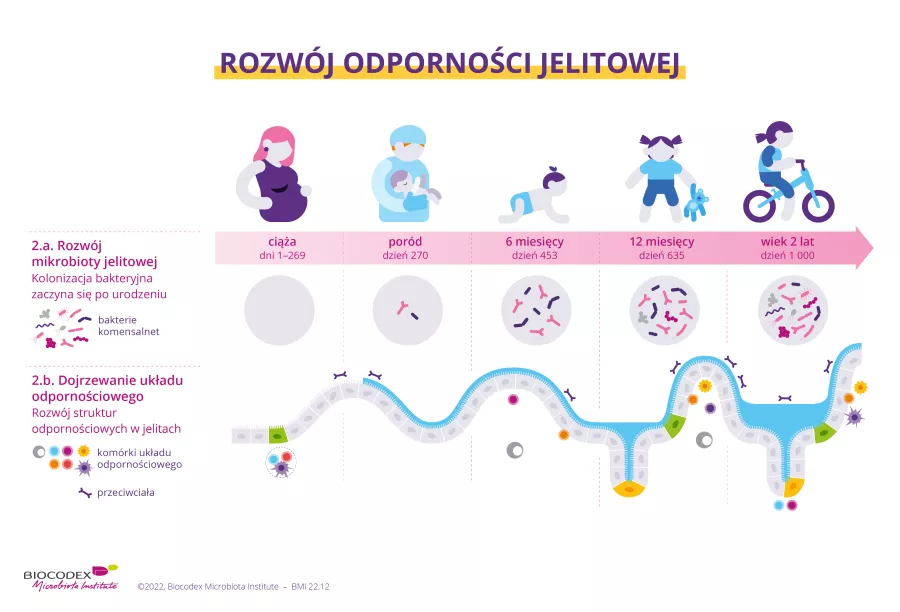
 Poznanie złożonych powiązań miedzy mikrobiota a odpornoscia to dopiero poczatek
Poznanie złożonych powiązań miedzy mikrobiota a odpornoscia to dopiero poczatek