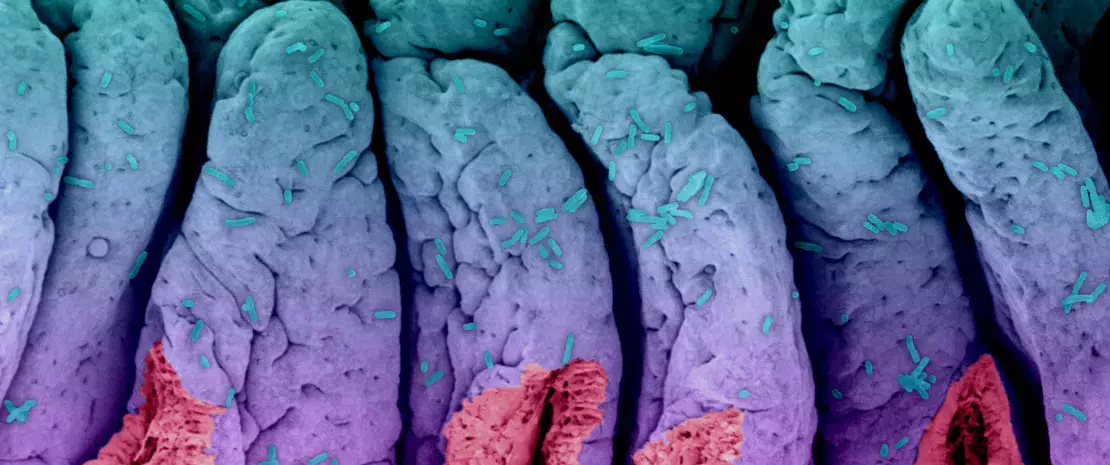
Woda pitna – źródło życia i... mikroorganizmów
Woda z kranu zawiera mikroorganizmy, które po spożyciu mogą skolonizować nasze jelita i wywrzeć wpływ na naszą mikrobiotę jelitową. Jednak większości z nich jeszcze nie znamy.
Mikrobiota jelit
Woda z kranu zawiera mikroorganizmy, które po spożyciu mogą skolonizować nasze jelita i wywrzeć wpływ na naszą mikrobiotę jelitową. Jednak większości z nich jeszcze nie znamy.
Mikrobiota jelit
Czyżby rośliny dobrze wpływały na skórę? A na naszą odporność? Nie – nie chodzi o krem z hamamelisem ani o olej ze słodkich migdałów, tylko o ściany wewnętrzne pokryte roślinami. Pewne badanie wykazało, że ich instalacja w miejscu pracy ma nie tylko zaletę ekologiczną. Ściany te przyczyniają się do równowagi mikrobioty skórnej i do regulacji układu odpornościowego pracowników.
Mikrobiota skóry Egzema
Nawet u zdrowych ochotników krótkie leczenie antybiotykami wystarczy, żeby wywołać zaburzenia mikrobioty jelitowej. Leczenie takie może również zostawić bardziej lub mniej trwałe „blizny” i trwałą oporność.

Jedna terapia antybiotykowa wystarczy, żeby trwale zaburzyć mykobiotę niemowląt. Jak? Niewątpliwie za pośrednictwem mikrobioty bakteryjnej. Proces ten może mieć długofalowe konsekwencje zdrowotne. Wyjaśniamy, jakie.
Aktualności, akredytowane szkolenia, infografiki, filmy z udziałem ekspertów, folder tematyczny... Rzućmy okiem na materiały Biocodex Microbiota Institute poświęcone dysbiozie, między innymi dysbiozie poantybiotykowej. Adekwatne do Twoich potrzeb zawodowych narzędzia i treści pozwalające Ci podnieść poziom wiedzy i bez trudu zostać ekspertem w zakresie dysbiozy!
Idź za przewodnikiem.

 Infografiki dla Twoich pacjentów
Infografiki dla Twoich pacjentów
 Posocznica noworodków: mikrobiota drogo płaci za stosowanie antybiotyków
Posocznica noworodków: mikrobiota drogo płaci za stosowanie antybiotyków
Od 4 do 10%1,2 populacji świata jest dotknięte zespołem jelita drażliwego (IBS), którego mechanizmy fizjopatologiczne wciąż pozostają niewyjaśnione. Badano już związek mikrobioty jelitowej z tym schorzeniem, ale nie znaleziono jednoznacznej korelacji. Zespół chińskich badaczy chciał dowiedzieć się więcej na ten temat.
 Zespół jelita drażliwego: czy przeszczep mikrobioty jelitowej jest skuteczny w długim terminie?
Zespół jelita drażliwego: czy przeszczep mikrobioty jelitowej jest skuteczny w długim terminie?
 Mikrobiota jelitowa: wspólny mianownik zaburzeń psychiatrycznych?
Mikrobiota jelitowa: wspólny mianownik zaburzeń psychiatrycznych?
Lato równa się wakacje, ale Twoja mikrobiota nie bierze urlopu. Możliwe nawet, że ciężko pracuje, kiedy Ty masz wolne.
Jaki wpływ – dobry albo zły – na Twoje zdrowie ma słońce? Chcesz się dowiedzieć, dlaczego komary kąsają Cię częściej niż sąsiada? Gdy jest ciepło, pocisz się. To normalne. Być może jednak zastanawiasz się, dlaczego w okresie dojrzewania zapach potu robi się przykry.
Odpowiedzi na swoje pytania znajdziesz w naszych specjalnych artykułach o mikrobiocie w lecie, które zamieszczamy poniżej.

Lato się kończy… Czas wrócić do dobrych nawyków, żeby dobrze przygotować się do powrotu do pracy lub szkoły. Może mikrobiota też gra w tym jakąś rolę?
Żywienie, sen, odporność... Przeczytaj nasze artykuły, które pomogą Ci wrócić do właściwego rytmu życia i zrealizować powakacyjne cele.

Skorzystaj z letniego urlopu, żeby skorzystać z uzdrawiającej mocy natury i wziąć porządny łyk świeżego powietrza! Twoja mikrobiota będzie Ci wdzięczna!
Czy wiesz, że...? Przyroda, zanieczyszczenia i Twój styl życia mogą wpływać na skład Twojej mikrobioty i, co za tym idzie, na stan Twojego zdrowia.
Zapraszamy do zapoznania się z naszymi artykułami, które sprawią, że jeszcze chętniej wybierzesz się w plener!

Czy jelita łączy z pęcherzem moczowym jakaś oś, która ma znaczenie dla nawrotów infekcji dróg moczowych? Jak działa? Poprzez dysbiozę jelit i nieskuteczną odpowiedź immunologiczną podczas kolonizacji pęcherza moczowego przez bakterie.
Wyjaśniamy.